Đốt một mẫu than đá nặng 0,6 gam trong không khí (dư) thu được 1,06 lít khí cacbonic . Tính thành phần phần trăm theo khối lượng cacbon trong mẫu than đá trên.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


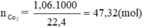
C + O2 → CO2
47,32 ← 47,32 (mol)
Theo pt: nC = nCO2 = 47,32 mol ⇒ mC = 47,32. 12 = 567,84 g
% khối lượng của C là:


C + O2 CO2
1,00mol 1,00mol
47,3 mol = 47,3 (mol)
Phần trăm khối lượng của C trong mẫu than đá: = 94,6%

C + O2 => CO2
1,06m3 = 1060 (l) => nCO2 = \(\frac{1060}{22,4}=47,32mol\)
nC = nCO2 = 47,32 mol
=> mC = 47,32.12 = 567,84 (g)
m than đá = 0,6kg = 600g
=> % C = \(\frac{567,84}{600}.100\%\) = 94,64%
C + O2 CO2
1,00mol 1,00mol
47,3 mol = 47,3 (mol)
Phần trăm khối lượng của C trong mẫu than đá: = 94,6%

a)
\(n_{CO_2}=\dfrac{16,8}{22,4}=0,75\left(mol\right)\)
PTHH: C + O2 --to--> CO2
0,75<-0,75<-----0,75
=> Độ tinh khiết = \(\%C=\dfrac{0,75.12}{10}.100\%=90\%\)
b)
\(n_{SO_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\)
PTHH: S + O2 --to--> SO2
0,025<-0,025<---0,025
=> \(V_{O_2\left(PTHH\right)}=\left(0,025+0,75\right).22,4=17,36\left(l\right)\)
=> \(V_{O_2\left(tt\right)}=\dfrac{17,36.110}{100}=19,096\left(l\right)\)

C + O2 →( t∘) CO2
1,00mol 1,00mol
47,3 mol \(\dfrac{1,06\cdot10^3}{22,4}\) = 47,3 (mol)
Phần trăm khối lượng của C trong mẫu than đá: \(\dfrac{47,3\cdot12,0\cdot100}{600}\) = 94,6%

có nhiều nguyên nhân
do gia tăng dân số ,cháy rừng ,khí thải
mik nghĩ rằng do hô hấp ở người và động thưc vật
khi đốt cháy 1 tấn than đá thì ít nhất phải sinh ra từ 1m3 đến 1.5m3
cần giảm thiểu số lượng tránh gia tăng dân số khí thải công nghiệp cần hạn chế việc phá rwungf đốt rừng có ảnh hưởng lớn



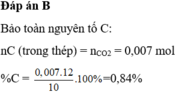
C + O2 \(\xrightarrow[]{t^o}\) CO2
nCO2 = \(\dfrac{1,06}{22,4}\approx0,047mol\)
Theo pt: nC = nCO2 = 0,047 mol
=> mC = 0,047.12 = 0,564g
%mC = \(\dfrac{0,564}{0,6}.100\%=94\%44\)
$C + O_2 \xrightarrow{t^o} CO_2$
n C = n CO2 = 1,06/22,4 = 53/1120(mol)
m C = 53/1120 .12 = 0,568(gam)
Suy ra :
%C = 0,568/0,6 .100% =94,67%