Đốt cháy 19.5 gam một kim loại R ( có hóa trị x, với x< hoặc = 3) sau một thời gian được 22,7 gam HHA gồm 2 chất rắn. Cho A tác dụng với dung dịch HCl dư thì thu được 2,24 lít H2 ( ở đktc). Xác định tên R?
Ai giải giùm mình thì mình con ơn nhiều nhá!




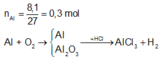
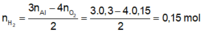
Bảo toàn khối lượng :
m O2 = 22,7 - 19,5 = 3,2(gam)
n O2 = 3,2/32 = 0,1(mol)
A gồm R2Ox và R dư
n H2 = 2,24/22,4 = 0,1(mol)
$4R + xO_2 \xrightarrow{t^o} 2R_2O_x$
$2R + 2xHCl \to 2RCl_x + xH_2$
Theo PTHH :
n R = 4/x .n O2 + 2/x . n H2 = 0,6/x(mol)
=> R.0,6/x = 19,5
<=> R = 65x/2
Với x = 2 thì R = 65(Zn)
Vậy R là kẽm