Nung 6,72 g Fe trong không khí thu được sắt (II) oxit FeO. Khối lượng FeO thu được và thể tích khí O2 phản ứng là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, \(FeO+H_2\underrightarrow{t^o}Fe+H_2O\)
b, \(n_{FeO}=\dfrac{7,2}{72}=0,1\left(mol\right)\)
\(n_{Fe}=n_{FeO}=0,1\left(mol\right)\Rightarrow m_{Fe}=0,1.56=5,6\left(g\right)\)
c, \(n_{H_2}=n_{FeO}=0,1\left(mol\right)\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)

a. PTHH: \(2Fe+O_2\rightarrow^{t^o}2FeO\)
\(4Fe+3O_2\rightarrow^{t^o}Fe_2O_3\)
\(3Fe+2O_2\rightarrow^{t^o}Fe_3o_4\)
b. Bảo toàn khối lượng \(m_{Fe}+m_{O_2}=m_{Oxit}\)
\(\rightarrow m_{O_2}=37,6-28=9,6g\)
\(\rightarrow n_{O_2}=\frac{9,6}{32}=0,3mol\)
\(\rightarrow V_{kk}=\frac{0,3.22,4}{20\%}=33,6\)

\(n_{Cu}=\dfrac{6,4}{64}=0,1mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,1 0,1 ( mol )
\(\left\{{}\begin{matrix}m_{CuO}=0,1.80=8g\\m_{FeO}=12-8=4g\end{matrix}\right.\)

a)
FeO + H2 --to--> Fe + H2O
CuO + H2 --to--> Cu + H2O
b) \(n_{Cu}=\dfrac{6,4}{64}=0,1\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
0,1<--0,1<-----0,1
=> \(m_{FeO}=12-0,1.80=4\left(g\right)\)
=> \(n_{FeO}=\dfrac{4}{72}=\dfrac{1}{18}\left(mol\right)\)
FeO + H2 --to--> Fe + H2O
\(\dfrac{1}{18}\)-->\(\dfrac{1}{18}\)----->\(\dfrac{1}{18}\)
=> \(V_{H_2}=\left(0,1+\dfrac{1}{18}\right).22,4=\dfrac{784}{225}\left(l\right)\)
c) \(m_{Fe}=\dfrac{1}{18}.56=\dfrac{28}{9}\left(g\right)\)
d) \(\left\{{}\begin{matrix}m_{CuO}=0,1.80=8\left(g\right)\\m_{FeO}=4\left(g\right)\end{matrix}\right.\)

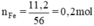
Phương trình hóa học của phản ứng:
Fe2O3 + 3H2 → 2Fe + 3H2O.
Khử 1 mol Fe2O3 cho 2 mol Fe.
x mol Fe2O3 → 0,2 mol.
x = 0,2 : 2 =0,1 mol.
m = 0,1 .160 =16g.
Khử 1 mol Fe2O3 cần 3 mol H2.
Vậy khử 0,1 mol Fe2O3 cần 0,3 mol H2.
V= 0,3 .22.4 = 6,72l.

hình như bn ghi sai r đó phải là:đồng oxit mới phải chứ![]()

Ta có: \(n_{Fe}=\dfrac{6,72}{56}=0,12\left(mol\right)\)
PT: \(2Fe+O_2\underrightarrow{t^o}2FeO\)
Theo PT: \(\left\{{}\begin{matrix}n_{FeO}=n_{Fe}=0,12\left(mol\right)\\n_{O_2}=\dfrac{1}{2}n_{Fe}=0,06\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{FeO}=0,12.72=8,64\left(g\right)\)
\(V_{O_2}=0,06.24,79=1,4874\left(l\right)\)