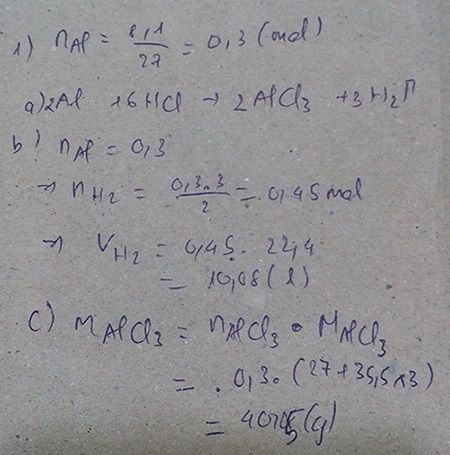Cho 8,1 g Al tác dụng vừa đủ với dung dịch HCL thu được muối AlCl³ và khí hydrogen
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Bài 8:
\(n_{H_2}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
_____0,2______0,6_____0,2____0,3 (mol)
a, \(m_{Al}=0,2.27=5,4\left(g\right)\)
b, \(C_{M_{HCl}}=\dfrac{0,6}{0,3}=2\left(M\right)\)
c, \(C_{M_{AlCl_3}}=\dfrac{0,2}{0,2}=1\left(M\right)\)
Bài 9:
Ta có: \(n_{H_2}=\dfrac{2,479}{24,79}=0,1\left(mol\right)\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
a, \(n_{Mg}=n_{H_2}=0,1\left(mol\right)\Rightarrow m_{Mg}=0,1.24=2,4\left(g\right)\)
\(\Rightarrow m_{MgO}=8,4-2,4=6\left(g\right)\)
b, \(n_{MgO}=\dfrac{6}{40}=0,15\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{Mg}+2n_{MgO}=0,5\left(mol\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{0,5.36,5}{3,65\%}==500\left(g\right)\)

a) PT: Fe+2HCl→FeCl2+H2 (1)
- Số mol Fe là:
nFe=\(\dfrac{m}{M}\)=\(\dfrac{11,2}{56}\)=0,2(mol)
- Theo PT (1)⇒nFeCl2=nFe=0,2(mol)
- Vậy khối lượng của FeCl2 là:
mFeCl2=n.M=0,2.127=25,4(g)
b) Theo PT (1)⇒nH2=nFe=0,2(mol)
- Vậy thể tích của H2 là:
VH2=n.24,79=0,2.24,79=4,958(l)
`#3107.101107`
`a)`
\(\text{Fe + 2HCl}\rightarrow\text{FeCl}_2+\text{H}_2\)
n của Fe có trong phản ứng là:
\(\text{n}_{\text{Fe}}=\dfrac{\text{m}_{\text{Fe}}}{\text{M}_{\text{Fe}}}=\dfrac{11,2}{56}=0,2\left(\text{mol}\right)\)
Theo PT: \(\text{n}_{\text{Fe}}=\text{n}_{\text{ }\text{FeCl}_2}=0,2\left(\text{mol}\right)\)
m của FeCl2 có trong phản ứng là:
\(\text{m}_{\text{FeCl}_2}=\text{n}_{\text{FeCl}_2}\cdot\text{M}_{\text{FeCl}_2}=0,2\cdot\left(56+35,5\cdot2\right)=25,4\left(\text{g}\right)\)
`b)`
Theo PT: \(\text{n}_{\text{Fe}}=\text{n}_{\text{H}_2}=0,2\left(\text{mol}\right)\)
V của khí H2 ở đkc là:
\(\text{V}_{\text{H}_2}=\text{n}_{\text{H}_2}\cdot24,79=0,2\cdot24,79=4,958\left(\text{l}\right)\)`.`

\(n_{HCl}=1,5.0,4=0,6(mol)\\ X+HCl\to muối+H_2\)
Bảo toàn H: \(n_{H_2}=\dfrac{n_{HCl}}{2}=0,3(mol)\)
\(\Rightarrow V_{H_2}=0,3.22,4=6,72(l)\\BTKL:m_A+m_{HCl}=m_{muối}+m_{H_2}\\ \Rightarrow m_{muối}=35+0,6.36,5-0,3.2=56,3(g)\)

2Al + 6HCl → 2AlCl3 + 3H2
2 6 2 3
0,3 0,9 0,3 0,45
a). nAl= \(\dfrac{8,1}{27}\)=0,3(mol)
⇒ nHCl= \(\dfrac{0,3.3}{6}\)= 0,9(mol).
⇒ mHCl=n.M= 0,9 . 36.5 =32,85(g).
b). nAlCl3= \(\dfrac{0,9.2}{6}\)= 0,3(mol).
⇒mAlCl3= n.M = 0,3 . 133,5 =40,05(g).
c). nH2= \(\dfrac{0,3.3}{2}\)= 0,45(mol).
⇒VH2= n . 22,4 = 0,45 . 22,4= 10,08(g).

a: \(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
0,2 0,4 0,2 0,2
\(V_{H_2}=0,2\cdot22,4=4,48\left(lít\right)\)
b: \(\dfrac{n_{HCl}}{V_{HCl}}=2\)
=>\(\dfrac{0.4}{V_{HCl}}=2\)
=>\(V_{HCl}=\dfrac{0.4}{2}=0.2\left(lít\right)\)
c: \(C_M=\dfrac{n}{V}=\dfrac{0.2}{0.2}=1\)

a) nAl = 43,2/27 = 1,6 mol
2Al + 6HCl → 2AlCl3 + 3H2
1,6 \(\dfrac{1,6\times3}{2}=2,4\)
→ nH2 = 2,4 mol → VH2 = 2,4 x 22, 4 = 53,76 lít
b) nCuO = 64/80 = 0,8 mol
nH2 = 2,4 mol
→ H2 dư, phương trình tính theo số mol của CuO
CuO + H2 → Cu + H2O
0,8 0,8 0,8 0,8
Chất rắn sau phản ứng có Cu
mCu = 0,8 x 64 = 51,2 gam