cho 24,5 g hỗn hợp A gồm Fe Cu Fe Ag tác dụng vừa hết với V ml dung dịch HNO3 1,6M thu được dung dịch B chứa m gam hỗn hợp muối nitrat và 6,272 lít NO Tính giá trị của m và V
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


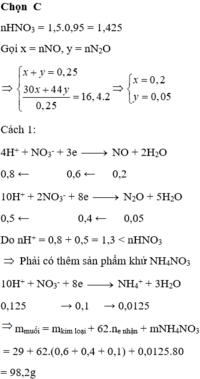
nHNO3 ban đầu = 1,425
MX = 32,8; Sử dụng sơ đồ đường chéo ⇒ n NO = 0,2 ; n N2O = 0,05
Ta có nNO3- trong muối kl = ne = 8nN2O + 8nNH4NO3
Bảo toàn nguyên tố N: nHNO3 ban đầu = n NO + 2n N2O + 2n NH4NO3 + n NO3- trong muối KL
⇒ nHNO3 ban đầu = 4 nNO + 10 nN2O + 10 nNH4NO3
⇒ nNH4NO3 = 0,0125
⇒ nNO3-/muối KL= 1,1
⇒ m = mNO3-/muối kl + mKL + mNH4NO3 = 1,1.62 +29 + 0,0125.80 = 98,2g
Đáp án A.

nHNO3 ban đầu = 1,425
MX = 32,8; Sử dụng sơ đồ đường chéo ⇒ n NO = 0,2 ; n N2O = 0,05
Ta có nNO3- trong muối kl = ne = 8nN2O + 8nNH4NO3
Bảo toàn nguyên tố N: nHNO3 ban đầu = n NO + 2n N2O + 2n NH4NO3 + n NO3- trong muối KL
⇒ nHNO3 ban đầu = 4 nNO + 10 nN2O + 10 nNH4NO3
⇒ nNH4NO3 = 0,0125
⇒ nNO3-/muối KL= 1,1
⇒ m = mNO3-/muối kl + mKL + mNH4NO3 = 1,1.62 +29 + 0,0125.80 = 98,2g
Đáp án A.

Ta có: \(m_{H_2SO_4}=160.98\%=156,8\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{156,8}{98}=1,6\left(mol\right)\)
\(n_S=\dfrac{9,6}{32}=0,3\left(mol\right)\)
\(4H_2SO_4+6e\rightarrow3SO_4^{2-}+S+4H_2O\)
1,2_______________0,9___0,3 (mol)
\(2H_2SO_4+2e\rightarrow SO_4^{2-}+SO_2+2H_2O\)
0,4______________0,2_____0,2 (mol)
⇒ m muối = mA + mSO42- = 26,92 + (0,9 + 0,2).96 = 132,52 (g)
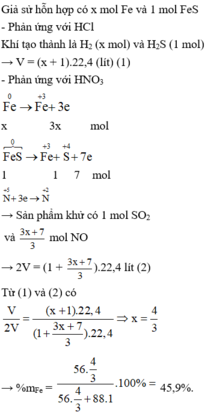

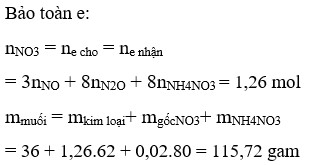
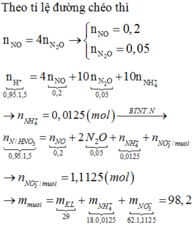

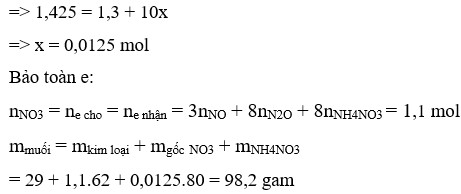


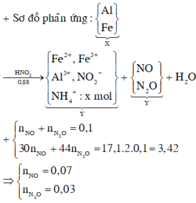

Fe tác dụng với HNO3 sẽ sinh ra Fe3+ em nha do HNO3 có tính oxi hóa mạnh nên sẽ đẩy Fe lên mức cao nhất
Sơ đồ:
\(24,5g\left(A\right)\left\{{}\begin{matrix}Fe\\Cu\\Ag\end{matrix}\right.\xrightarrow[1,6M]{+HNO_3}\left(B\right)\left\{{}\begin{matrix}Fe^{3+}\\Cu^{2+}\\Ag^+\\NO_3^-\end{matrix}\right.+NO:6,372l\)
\(n_{NO}=\dfrac{6,272}{22,4}=0,28mol\\ BTe:3n_{Fe}+2n_{Cu}+n_{Ag}=3n_{NO}=3.0,28=0,84mol\\ m=24,5+0,84.62=76,58g\)
\(BTNT\left(N\right):n_{HNO_3}=n_{NO_3^-}+n_{NO}\\ \Leftrightarrow n_{HNO_3}=0,84+0,28\\ \Leftrightarrow n_{HNO_3}=1,12mol\\ \\ V=V_{HNO_3}=\dfrac{1,12}{1,6}=0,7l=700ml\)