Khi làm thí nghiệm, làm thế nào để biết một phản ứng là tỏa nhiệt hay thu nhiệt?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


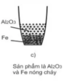
Thí nghiệm 2: Thu nhiệt
Thí nghiệm 3: Toả nhiệt
Phản ứng tỏa nhiệt là thí nghiệm 2, phản ứng thu nhiệt là thí nghiệm 3

C1. Trong thí nghiệm trên, yếu tố nào ở hai cốc được giữ giống nhau, yếu tố nào được thay đồi ? Tại sao phải làm như thế ? Hãy tìm số thích hợp cho các ô trống ở hai cột cuối bảng 24.1. Biết nhiệt lượng ngọn lửa đèn cồn truyền cho nước tỉ lệ với thời gian đun.
Bài giải:
Độ tăng nhiệt độ và chất làm vật được giữ giống nhau; khối lượng khác nhau. Để tìm hiểu mỗi quan hệ giữa nhiệt lượng và khối lượng.
C2. Từ thí nghiệm trên có thể kết luận gì về mỗi quan hệ giữa nhiệt lượng vật cần thu vào để nóng lên và khối lượng của vật ?
Bài giải:
Khối lượng càng lớn thì nhiệt lượng vật thu vào càng lớn.
C3. Trong thí nghiệm này phải giữ không đổi những yếu tố nào ? Muốn vậy phải làm thế nào ?
Bài giải:
Phải giữ khối lượng và chất làm vật giống nhau. Muốn vậy hai cốc phải đựng cùng một lượng nước.
C4. Trong thí nghiệm này phải thay đổi yếu tố nào ? Muốn vậy phải làm thế nào ?
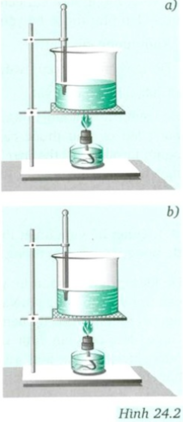
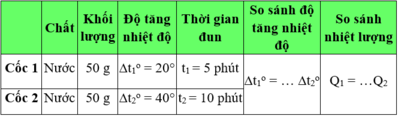
Sau đây là bảng kết quả thí nghiệm làm với hai cốc, mỗi cốc đựng 50 g nước, được lần lượt đun nóng bằng đền cồn trong 5 phút, 10 phút (H.24.2). Hãy tìm số thích hợp cho các ô trống ở hai cột cuối bảng 24.2.
Bài giải:
Phải cho độ tăng nhiệt độ khác nhau. Muốn vậy phải để cho nhiệt độ cuối của 2 cốc khác nhau bằng cách cho thời gian đun khác nhau.
C5. Từ thí nghiệm trên có thể rút ra kết luận gì về mỗi quan hệ giữa nhiệt lượng vật thu vào để nóng lên và độ tăng nhiệt độ ?
Bài giải:
Độ tăng nhiệt độ càng lớn thì nhiệt lượng vật thu vào càng lớn.
C6. Trong thí nghiệm này những yếu tố nào thay đổi, không thay đổi ?
Bài giải:
Khối lượng không đổi, độ tăng nhiệt độ giống nhau, chất làm vật khác nhau.

* Cần phải thay đổi độ tăng nhiệt độ của hai cốc khác nhau. Muốn vậy thời gian đun hai cốc phải khác nhau.
* Kết quả ghi ở bảng 24.2
Ta có: Δt1o = 1/2 .Δt2o và Q2 = 1/2 .Q1

Để kiểm tra tốc độ bay hơi của một chất lỏng phụ thuộc vào các yếu tố: nhiệt độ, gió, mặt thoáng thì phải làm với cùng một chất lỏng nhưng thực hiện ở các điều kiện nhiệt độ, gió, mặt thoáng khác nhau
⇒ Đáp án C

\(V_{O_2\left(thu.được\right)}=28=0,1=2,8\left(l\right)\)
=> \(V_{O_2\left(sinh.ra\right)}=\dfrac{2,8.100}{80}=3,5\left(l\right)\)
=> \(n_{O_2\left(sinh.ra\right)}=\dfrac{3,5}{22,4}=0,15625\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,3125<------------------------0,15625
=> mKMnO4 = 0,3125.158 = 49,375 (g)

\(a.E_r=839,0+2\cdot418,4+2\cdot432,0=2539,8kJ\\ b.E_p=343,3+6\cdot418,4=2853,7kJ\\ c.\Delta_rH^{^{ }0}=2539,8-3197=-313,9kJ\cdot mol^{-1}\\ \Delta H< 0:pư.thu.nhiệt\)
\(a.E_{reactants}=839,0+2\cdot432,0=1703kJ\\ b.E_{products}=343,3+6\cdot432,0=2935,3kJ\\ c.\Delta_rH^{^o}_{298}=E_r-E_p=1703-2935,3=1232,3kJ\cdot mol^{^{ }-1}.\)
\(\Delta H< 0\) => Phản ứng (1) thu nhiệt

Chọn B
Thay O2 không khí bằng O2 tinh khiết là làm tăng nồng độ của O2. Trường hợp này cân bằng chuyển dịch theo chiều thuận, do đó làm tăng hiệu suất của phản ứng.
Tăng áp suất thì cân bằng hóa học sẽ chuyển dịch theo chiều làm giảm số phân tử khí, tức là chiều thuận, do đó cũng làm tăng hiệu suất tổng hợp SO3.
Chất xúc tác không làm ảnh hưởng đến sự chuyển dịch cân bằng, nó chỉ giúp cho cân bằng nhanh chóng được thiết lập.
Tăng nhiệt độ thì cân bằng sẽ chuyển dịch theo chiều thu nhiệt, tức là chiều nghịch, do đó làm giảm hiệu suất phản ứng.
Vậy các biện pháp (a) và (b) là tăng hiệu suất phản ứng

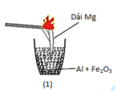

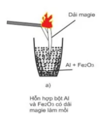
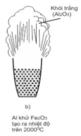
- Để nhận biết phản ứng tỏa nhiệt: Ta cảm nhận hoặc đo được nhiệt độ xung quanh phản ứng thí nghiệm đó tăng lên . Hoặc phản ứng không cần cung cấp nhiệt trong suốt quá trình xảy ra phản ứng
- Để nhận biết phản ứng thu nhiệt: Ta cần phải cung cấp nhiệt trong suốt quá trình xảy ra phản ứng thì phản ứng mới diễn ra