Vì sao HF có tính acid yếu hơn rất nhiều so với HCl? Biết rằng tính acid của một chất càng mạnh nếu phân tử đó càng dễ phân li thành ion H+.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(\text{#TNam}\)
`a,` Gọi `NTK` của Sulfur là `x`
Ta có: `PTK= 2*1+x+16*4=98 <am``u>`
`2+x+64=98`
`-> 2+x=98-64`
`->2+x=34`
`-> x=34 - 2`
`-> x= 32 <am``u>`
Vậy, `NTK` của \(\text{Sulfur}\) là `32 am``u.`
`b,` Phân tử \(\text{Sulfuric acid}\) là hợp chất
Vì phân tử \(\text{Sulfuric acid}\) được cấu tạo từ `3` nguyên tố hóa học.

- Tính acid phụ thuộc vào khả năng tách H của acid. Phân tử nào càng dễ tách H thì tính acid càng mạnh
- Trong nhóm halogen, từ F đến I có độ âm điện giảm dần
=> Khả năng liên kết H-X giảm dần
=> Khả năng tách H trong HX tăng dần
=> Tính acid tăng dần
=> Dung dịch HF có tính acid yếu nhất

Tham khảo:
- Trong dung dịch nước, chỉ một phần nhỏ carboxylic acid phân li thành ion, vì vậy carboxylic là những acid yếu. Tuy nhiên, chúng thể hiện đầy đủ các tính chất của một acid:
+ Tác dụng với kim loại đứng trước hydrogen trong dãy hoạt động hoá học của kim loại và giải phóng khí hydrogen.
+ Tác dụng được với các base và basic oxide để tạo thành muối và nước.
+ Tác dụng được với một số muối.

Tính chất của các chất phụ thuộc vào thành phần phân tử (loại nguyên tố, số lượng nguyên tử) và cấu tạo hoá học (trật tự liên kết của các nguyên tử với nhau). Cụ thể ở đây :
- Acetic acid (CH3COOH): có 2 nguyên tử C liên kết với nhau (C - C).
- Methyl fomate (HCOOCH3): có 2 nguyên tử C liên kết với nguyên tử O (C - O - C)
Vì thế nên mặc dù có cùng công thức phân tử C2H4O2 nhưng acetic acid có tính chất khác với methyl formate.

Tham khảo:
Tính chất của các chất phụ thuộc vào thành phần phân tử (loại nguyên tố, số lượng nguyên tử) và cấu tạo hoá học (trật tự liên kết của các nguyên tử với nhau). Do đó dù có cùng công thức phân tử C2H4O2 nhưng acetic acid có tính chất khác với methyl formate do cấu tạo hoá học khác nhau.


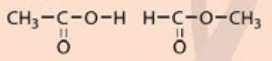
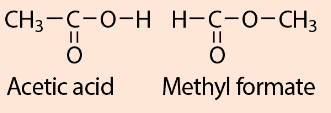
- Tính acid của một chất càng mạnh nếu phân tử đó càng dễ phân li thành ion H+.
⟹ HF khó phân li thành ion H+ hơn so với HCl.
- Các phân tử hydrogen halide thì chỉ HF có liên kết hydrogen, các liên kết này sẽ làm cho nguyên tử H bị giữ chặt hơn ⟹ Khó tách ion H+ hơn so với HCl.
Vì vậy tính acid của HF yếu hơn rất nhiều so với HCl.