Câu 11. Hòa tan 16 gam SO3 trong nước thu được 250 ml dung dịch H2SO4 x M. Tìm giá trị của x.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

`C1:`
`2NaOH+H_2 SO_4 ->Na_2 SO_4 +2H_2 O`
`n_[H_2 SO_4]=0,2.1=0,2(mol)`
`n_[NaOH]=[200.10]/[100.40]=0,5(mol)`
Ta có: `[0,2]/1 < [0,5]/2=>NaOH` dư, `H_2 SO_4` hết.
`=>` Quỳ tím chuyển xanh.
`C2:`
`SO_3 +H_2 O->H_2 SO_4`
`0,2` `0,2` `(mol)`
`n_[SO_3]=16/80=0,2(mol)`
`C_[M_[H_2 SO_4]]=[0,2]/[0,25]=0,8(M)`

Ta có: \(n_{SO_3}=\dfrac{16}{80}=0,2\left(mol\right)\)
PTHH: SO3 + H2O ---> H2SO4
Theo PT: \(n_{H_2SO_4}=n_{SO_3}=0,2\left(mol\right)\)
Đổi 250ml = 0,25 lít
\(\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,2}{0,25}=0,8M\)
Chọn B

Đáp án C
Các phản ứng: Na + H2O → NaOH + ½ H2
2NaOH + H2SO4 → Na2SO4 + 2H2O
nH2SO4 = 0,1.1 = 0,1 mol
Theo các phản ứng: nNa = nNaOH = 2nH2SO4 = 0,2 mol
=> mNa = m = 23.0,2 = 4,6g

Đáp án D.
![]()
![]()
Zn + H2SO4 → ZnSO4 + H2
0,1 → 0,1 → 0,1
H2SO4 + Ba(OH)2 → BaSO4 + 2H2O
0,3 → 0,3 → 0,4
ZnSO4 + Ba(OH)2 → BaSO4 + Zn(OH)2
0,1 0,25 → 0,1 → 0,1
Zn(OH)2 + Ba(OH)2 → BaZnO2 + 2H2O
0,1 0,15
Kết tủa thu được gồm 0,4 mol BaSO4: m = 0,4.233 = 93,2 gam
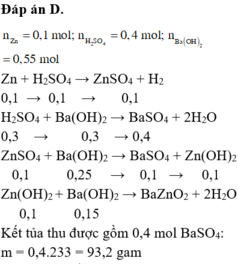
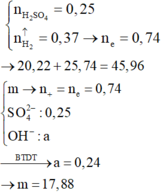
\(n_{SO_3}=\dfrac{16}{80}=0,2\left(mol\right)\)
PT: \(SO_3+H_2O\rightarrow H_2SO_4\)
Theo PT: \(n_{H_2SO_4}=n_{SO_3}=0,2\left(mol\right)\Rightarrow x=C_{M_{H_2SO_4}}=\dfrac{0,2}{0,25}=0,8\left(M\right)\)