cho 5,4 AL vào 200ml dd HCL sau phản ứng thu được V lít H2(đktc) a) tính giá trị V b) tính nồng độ CM của dung dịch HCl phản ứng Giúp mik vs ạ nếu có giải thì hãy giải giúp mik làm đầy đủ với ạ,mik c.ơn
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
nAl = 0,2, nFe = 0,1 (mol)
2Al + 6HCl→ 2AlCl3 + 3H2
0,2 → 0,3 (mol)
Fe + 2HCl→ FeCl2 + H2
0,1 0,1 (mol)
V = (0,3+0,1).22,4 = 8,96 (l)

\(n_{Mg}=0,3\left(mol\right)\)
\(n_{HCl}=0,3\left(mol\right)\)
\(PTHH:Mg+2HCl\rightarrow MgCl_2+H_2\)
...............0,15......0,3..........0,15.....0,15......
- Thấy sau phản ứng HCl phản ứng hết, Mg còn dư ( dư 0,15 mol )
\(\Rightarrow\left\{{}\begin{matrix}m_M=m_{MgCl_2}=14,25\left(g\right)\\V=V_{H_2}=3,36\left(l\right)\end{matrix}\right.\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
Ta có: \(n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
\(n_{HCl}=0,2.1,5=0,3\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,3}{2}\), ta được Mg dư.
Theo PT: \(n_{MgCl_2}=n_{H_2}=\dfrac{1}{2}n_{HCl}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{MgCl_2}=0,15.95=14,25\left(g\right)\\V_{H_2}=0,15.22,4=3,36\left(l\right)\end{matrix}\right.\)
Bạn tham khảo nhé!

a)Gọi x,y lần lượt là số mol của Al, Fe trong hỗn hợp ban đầu (x,y>0)
Sau phản ứng hỗn hợp muối khan gồm: \(\left\{{}\begin{matrix}AlCl_3:x\left(mol\right)\\FeCl_2:y\left(mol\right)\end{matrix}\right.\)
Ta có hệ phương trình: \(\left\{{}\begin{matrix}27x+56y=13,9\\133,5x+127y=38\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x\approx0,0896\\y\approx0,205\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,0896\cdot27\cdot100\%}{13,9}\approx17,4\%\\\%m_{Fe}=\dfrac{0,205\cdot56\cdot100\%}{13,9}\approx82,6\%\end{matrix}\right.\)
Theo Bảo toàn nguyên tố Cl, H ta có:\(n_{H_2}=\dfrac{n_{HCl}}{2}=\dfrac{3n_{AlCl_3}+2n_{FeCl_2}}{2}\\ =\dfrac{3\cdot0,0896+2\cdot0,205}{2}=0,3394mol\\ \Rightarrow V_{H_2}=0,3394\cdot22,4\approx7,6l\)

\(\text{Ta có PTHH}\\2Al+6HCl \rightarrow 2AlCl_3+3H_2 \uparrow\\n_{Al}=\dfrac{5,4}{27}=0,2(mol)\\\Rightarrow n_{HCl}=3n_{Al}=0,6(mol)\\\Rightarrow C_{M_{HCl}}=n/V=\dfrac{0,6}{0,15}=4(M)\\\text{ Câu hỏi 1 : B}\\\Rightarrow n_{AlCl_3}=n_{Al}=0,2(mol)\\\Rightarrow m_{AlCl_3} = 0,2.133,5=26,7(gam)\\\text{ Câu hỏi 2 : A}\\\Rightarrow n_{H_2}=3/2n_{Al}=0,3(mol)\Rightarrow V_{H_2}(đktc)=0,3.22,4=6,72(lít)\\\text{ Câu hỏi 3 : C} \)

Muối = Kim loại + gốc Cl
➝ Khối lượng của gốc Cl là: mCl = 49,8 - 14,3 = 35,5 gam
➝ nCl = nHCl = 35,5/35,5 = 1 mol
Khi viết phương trình ra sẽ thấy mối liên hệ: nHCl = 2nH2
➝ nH2 = 0,5 mol ➝ VH2 = 0,5.22,4 = 11,2 lít
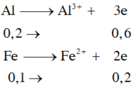
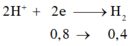

a: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2 0,6 0,2 0,3
\(V=0.3\cdot22.4=6.72\left(lít\right)\)
b: \(C_{M\left(HCL\right)}=\dfrac{0.6}{0.2}=3\left(M\right)\)