nguyên tử của nguyên tố X có phân lớp electron đang sắp xếp là 3s^1.số hiệu của nguyên tử X là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(X:\left[Ne\right]3s^23p^5\\ \sum hạt\left(điện\right)=2\left(2+8+7\right)=34\)

Đáp án C
TH1: Y có phân lớp ngoài cùng là 3s1
→ Y có cấu hình electron là 1s22s22p63s1
→ Y có 11e → Y có Z = 11.
X có số electron ở phân lớp ngoài cùng = 7 - 1 = 6
→ X có phân lớp ngoài cùng là 3p6 → X là khí hiếm → loại.
• TH2: Y có phân lớp ngoài cùng là 3s2 → tương tự ta có Y có Z = 12.
Khi đó, X có lớp ngoài cùng là 3p5
→ X có cấu hình electron là 1s22s22p63s23p5
→ X có 17 e → Z = 17.

C
TH1: Y có phân lớp ngoài cùng là 3 s 1 → Y có cấu hình electron là 1 s 2 2 s 2 2 p 6 3 s 1
→ Y có 11e → Y có Z = 11.
X có số electron ở phân lớp ngoài cùng = 7 - 1 = 6 → X có phân lớp ngoài cùng là 3 p 6 → X là khí hiếm → loại.
• TH2: Y có phân lớp ngoài cùng là 3 s 2 → Y có cấu hình electron là 1 s 2 2 s 2 2 p 6 3 s 2
→ Y có 12 electron → Y có Z = 12.
Khi đó, X có lớp ngoài cùng là 3 p 5 → X có cấu hình electron là 1 s 2 2 s 2 2 p 6 3 s 2 3 p 5
→ X có 17 e → Z = 17.

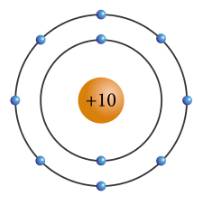
a: X có 10electron và có 2 lớp electron
b: X là neon
c: Oxy, Nitơ,cacbon

Đáp án D
Cấu hình electron của nguyên tố X, Y lần lượt là 1s22s22p63s23px và 1s22s22p63sy.
Ta có: x + y = 7.
• TH1: y = 1 → x = 6
→ Cấu hình electron của nguyên tố X, Y lần lượt là 1s22s22p63s23p6 và 1s22s22p63s1.
Mà X không phải là khí hiếm → loại.
• TH2: y = 2 → x = 5
→ Cấu hình electron của nguyên tố X, Y lần lượt là 1s22s22p63s23p5 và 1s22s22p63s2.
Vậy điện tích hạt nhân của X, Y lần lượt là X (17+) và Y (12+) → Chọn D.

\(X:\left[Ne\right]3s^1\\ Z_X=2+8+1=11\)