lam pp bao toan e giúp ạ
cần ? g đồng để khử hoàn toàn lượng bạc có trong 85ml dd AgNO3 0,15M ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

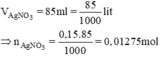
Phương trình hóa học của phản ứng:
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Theo pt:
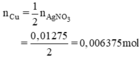
mCu tham gia phản ứng: 0,006375 × 64 = 0,408 g.

HD:
Cu + 2AgNO3 \(\rightarrow\) Cu(NO3)2 + 2Ag
Số mol Cu = 1/2 số mol AgNO3 = 0,15.0,085/2 = 0,006375 mol.
Khối lượng Cu = 0,006375.64 = 0.408 g.

\(m_{ct}=\dfrac{2,84.100}{100}=2,84\left(g\right)\)
\(n_{Na2SO4}=\dfrac{2,84}{142}=0,02\left(mol\right)\)
a) Pt ; \(Na_2SO_4+Ba\left(NO_3\right)_2\rightarrow2NaNO_3+BaSO_4|\)
1 1 2 1
0,02 0,02 0,04 0,02
b) \(n_{Ba\left(NO3\right)2}=\dfrac{0,02.1}{1}=0,02\left(mol\right)\)
\(m_{Ba\left(NO3\right)2}=0,02.261=5,22\left(g\right)\)
\(m_{ddBa\left(NO3\right)2}=\dfrac{5,22.100}{2,088}=250\left(g\right)\)
c) \(n_{NaNO3}=\dfrac{0,02.2}{1}=0,04\left(mol\right)\)
⇒ \(m_{NaNO3}=0,04.85=3,4\left(g\right)\)
\(n_{BaSO4}=\dfrac{0,04.1}{2}=0,02\left(mol\right)\)
⇒ \(m_{BaSO4}=0,02.233=4,66\left(g\right)\)
\(m_{ddspu}=100+250-4,66=345,34\left(g\right)\)
\(C_{NaNO3}=\dfrac{3,4.100}{345,34}=0,98\)0/0
Chúc bạn học tốt
a, \(n_{Na_2SO_4}=100.2,84\%=2,84\left(g\right)\Rightarrow n_{Na_2SO_4}=\dfrac{2,84}{142}=0,02\left(mol\right)\)
PTHH: Na2SO4 + Ba(NO3)2 → 2NaNO3 + BaSO4
Mol: 0,02 0,02 0,04 0,02
b,\(m_{ddBa\left(NO_3\right)_2}=\dfrac{0,02.261.100}{2,088}=250\left(g\right)\)
c, mdd sau pứ = 100+250-0,02.233 = 345,34 (g)
\(C\%_{ddNaNO_3}=\dfrac{0,04.85.100\%}{345,34}=0,98\%\)

Bài 1 :
Pt : \(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag|\)
1 2 1 2
x 0,2 2x
Gọi x là số mol của Cu
Vì khối lượng của đồng tăng so với ban đầu nên ta có phương trình :
\(m_{Ag}-m_{Cu}=15,2\left(g\right)\)
\(108.2x-64.x=15,2\)
\(216x-64x=15,2\)
\(152x=15,2\)
⇒ \(x=\dfrac{15,2}{152}=0,1\)
\(n_{AgNO3}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
500ml = 0,5l
\(C_{M_{ddAgNO3}}=\dfrac{0,2}{0,5}=0,4\left(M\right)\)
Chúc bạn học tốt

Bài 1:
\(PTHH:Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\\ \Rightarrow n_{Ag}=2n_{Cu}\\ m_{tăng}=m_{Ag}-m_{Cu}=15,2\left(g\right)\\ \Rightarrow108n_{Ag}-64n_{Cu}=15,2\\ \Rightarrow216n_{Cu}-64n_{Cu}=15,2\\ \Rightarrow n_{Cu}=0,1\left(mol\right)\\ \Rightarrow n_{AgNO_3}=0,2\left(mol\right)\\ \Rightarrow C_{M_{AgNO_3}}=\dfrac{0,2}{0,5}=0,4M\)
Bài 2:
\(n_A=\dfrac{78}{M_A}\left(mol\right);n_{ACl}=\dfrac{149}{M_A+35,5}\left(mol\right)\\ PTHH:2A+Cl_2\rightarrow2ACl\\ \Rightarrow n_A=n_{ACl}\Rightarrow\dfrac{78}{M_A}=\dfrac{149}{M_A+35,5}\\ \Rightarrow78M_A+2769=149M_A\\ \Rightarrow71M_A=2769\\ \Rightarrow M_A=39\\ \Rightarrow A\text{ là kali }\left(K\right)\)
Bài 3:
\(a,2Al+3ZnSO_4\rightarrow Al_2\left(SO_4\right)_3+3Zn\\ b,Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ MgO+H_2SO_4\rightarrow MgSO_4+H_2O\\ MgCO_3+H_2SO_4\rightarrow MgSO_4+H_2O+CO_2\uparrow\)

PTHH: \(KOH+HCl\rightarrow KCl+H_2O\)
\(KCl+AgNO_3\rightarrow KNO_3+AgCl\downarrow\)
Ta có: \(n_{HCl}=0,2\cdot2=0,4\left(mol\right)=n_{KOH}=n_{KNO_3}=n_{AgCl}\)
\(\Rightarrow\left\{{}\begin{matrix}m_{KOH}=0,1\cdot56=5,6\left(g\right)\\m_{AgCl}=0,1\cdot143,5=14,35\left(g\right)\\m_{KNO_3}=0,1\cdot101=10,1\left(g\right)\end{matrix}\right.\)
\(n_{AgNO_3}=0,085.0,15=0,01275\left(mol\right)\)
Theo ĐLBT e, có: 2nCu = nAg ⇒ nCu = 0,006375 (mol)
⇒ mCu = 0,006375.64 = 0,408 (g)
Pro lok
Quá trình:
\(Cu\rightarrow Cu^{+2}+2e\)
nCu____________2nCu (mol)
\(Ag^++e\rightarrow Ag\)
nAg+__nAg+ (mol)
Theo ĐLBT e, có: 2nCu = nAg+