1. Viết công thức electron, công thức Lewis và công thức cấu tạo của phân tử nitrogen.
2. Từ cấu tạo phân tử, hãy cho biết tại sao phân tử N2 có năng lượng liên kết lớn. Dự đoán về khả năng hoạt động hóa học của nitrogen ở nhiệt độ thường.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Viết CT electron và công thức cấu tạo của phân tử chứa liên kết cộng hoá trị: N 2 và H 2 O (1,0 điểm)


Ở trạng thái cơ bản, cả cacbon và oxi đều có 2 e độc thân ở phân lớp 2p. Do đó chúng có thể tạo thành 2 liên kết cộng hóa trị. Do oxi còn 1 cặp e chưa tham gia liên kết, cacbon còn orbital trống nên giữa chúng hình thành liên kết cho nhận
Vì cặp e từ oxi nên mũi tên của liên kết cho nhận có chiều từ oxi sang cacbon
Đáp án D

Tham khảo:
- CH4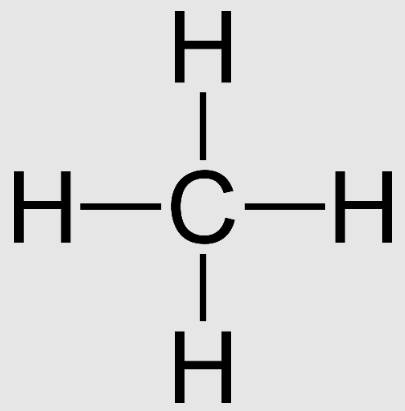
- C2H6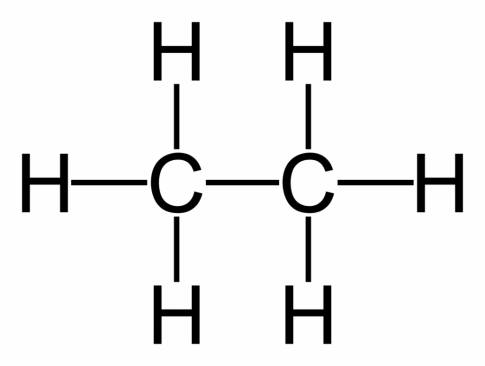
- C3H8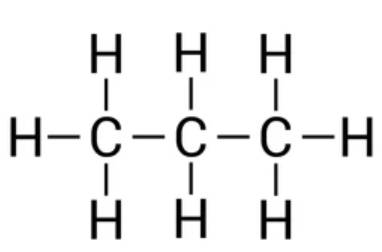
Trong phân tử alkane chỉ có các liên kết σ bền và kém phân cực. Mỗi nguyên tử carbon cũng như hydrogen đã tạo ra số liên kết cộng hoá trị lớn nhất của chúng. Vì thế, các alkane khó tham gia vào các phản ứng hoá học và phản ứng xảy ra sẽ kèm theo việc thay thế nguyên tử hydrogen hoặc bẻ gãy mạch carbon. Ở điều kiện thường, các alkane kém hoạt động, chúng không tác dụng với acid, kiềm và một số chất oxi hoá như dung dịch KMnO4, K2Cr2O7,... Các phản ứng tiêu biểu của alkane là phản ứng thế halogen (chlorine, bromine), phản ứng cracking, phản ứng reforming và phản ứng cháy.

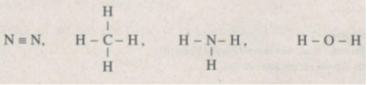
Các liên kết trong phân tử N 2 là các liên kết cộng hoá trị điển hình, không phân cực vì đó là những liên kết giữa hai nguyên tử giống nhau (hiệu độ im điện bằng không).
Các liên kết trong các phân tử còn lại là các liên kết giữa các nguyên tử trong cùng một chu kì (C, N, O) và nguyên tử H (độ âm điện bằng 2,20). ri trong cùng một chu kì, độ âm điện tăng dần từ trái sang phải nên so với H, hiệu độ âm điện cũng tăng theo, do đó các liên kết trong phân tử H 2 O là các liên kết phân cực mạnh nhất.

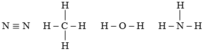
| N2 | CH4 | H2O | NH3 | |
| Hiệu độ âm điện | 0 | 0,35 | 1,24 | 0,84 |
Phân tử N2, CH4 có liên kết cộng hóa trị không phân cực. Phân tử H2O có liên kết cộng hóa trị phân cực mạnh nhất trong dãy.
1. Công thức electron, công thức Lewis và công thức cấu tạo của phân tử nitrogen lần lượt là:
\(:N:::N:\\ :N\equiv N:\\ N\equiv N\)
2.
\(E_b\left(N_2\right)\) lớn vì giữa hai nguyên tử N có liên kết ba bền.
Do đó, nitrogen khá trơ ở điều kiện thường.