Cho phản ứng đốt cháy 1 mol ethanol (C2H6O):
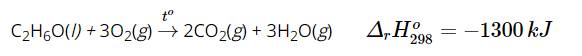
Phản ứng trên là phản ứng thu nhiệt hay tỏa nhiệt? Dự đoán về mặt năng lượng, phản ứng trên xảy ra thuận lợi hay không.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
- Xét phản ứng đốt cháy 1 mol C2H4
C2H4 (g) + 3O2 (g) → 2CO2 (g)+ 2H2O (g)
∆fH0298 = 1 x Eb (C2H4) + 3 x Eb (O2) - 2 x Eb (CO2) - 2 x Eb (H2O)
∆fH0298 = 1 x EC=C + 4 x EC-H + 3 x EO2 – 2 x 2EC=O – 2 x 2EO-H
∆fH0298 = 1x611 + 4x414 + 3x498 – 2x2x799 – 2x2x464 = -1291kJ
- Xét phản ứng đốt cháy 1 mol C2H6
C2H6 (g) + 7/2 O2 (g) → 2CO2 (g)+ 3H2O (g)
∆fH0298 = 1 x Eb (C2H6) + 7/2 x Eb (O2) - 2 x Eb (CO2) - 3 x Eb (H2O)
∆fH0298 = 1 x EC-C + 6 x EC-H + 7/2 x EO2 – 2 x 2EC=O – 3 x 2EO-H
∆fH0298 = 1x347 + 6x414 + 7/2 x498 – 2x2x799 – 3x2x464 = -1406kJ
- Xét phản ứng đốt cháy 1 mol CO
CO(g) + ½ O2 (g) → CO2(g)
∆fH0298 = 1 x Eb (CO) + 1/2 x Eb (O2) - 1 x Eb (CO2)
∆fH0298 = 1 x ECO + 1/2 x EO2 – 1 x 2EC=O
∆fH0298 = 1 x 1072 + 1/2 x 498– 1x2x799 = -277kJ
b)
F2(g) + H2O(g) → 2HF(g) + ½ O2 (g)
∆fH0298 = 1 x Eb (F2) + 1 x Eb (H2O) - 2 x Eb (HF) – 1/2 x Eb (O2)
∆fH0298 = 1 x EF-F + 1x2EO-H - 2 x EH-F - 1/2 x EO2
∆fH0298 = 1 x 159 + 2x464– 2x565 - 1/2 x 498= -292kJ
Các phản ứng trên đều có giá trị elthanpy âm => Các phản ứng trên đều thuận lợi

- Giá trị năng lượng liên kết của:
+ F – F trong phân tử F2: 159 kJ mol-1
+ N = N trong phân tử N2: 418 kJ mol-1
⟹ Năng lượng liên kết của F – F < N = N.
⟹ Liên kết của N2 bền hơn F2.
- Vậy phản ứng giữa F2 với H2 thuận lợi hơn (dễ xảy ra hơn) so với phản ứng giữa N2 với H2.

Đáp án B
Sản phẩm thu được là 2 hạt (k = 2) He.
Q = 1 k . N . ∆ E = 1 k . n . N A . ∆ E ≈ 1 , 69 . 10 24 M e V .

Giá trị \(\Delta H\) và \(S\) của từng nguyên tử, phân tử bạn ghi rõ ra giúp mình.
Hướng dẫn:
a. Xét \(\Delta H\) của phản ứng = \(\Delta H\) sinh của sản phẩm - \(\Delta H\) sinh của chất tham gia
Với \(\Delta H\) > 0 thì phản ứng thu nhiệt và \(\Delta H\) < 0 thì phản ứng tỏa nhiệt
b. Xét \(\text{}\Delta G=\Delta H-T\Delta S\)
Với \(\Delta S=Scủasảnphẩm-Scủachấtthamgia\)
Với \(\Delta G\) < 0 thì pư tự diễn biến tại điều kiện T đang xét
Và ngược lại.
À mà đây đâu phải chương trình hóa lớp 9 đâu nhỉ??! Bạn tính học đội tuyển hóa cấp 3 hả?

Đáp án C
1. Sai: cân bằng hóa học là cân bằng động
2. đúng: phản ứng nghịch thu nhiệt, khi tăng nhiệt độ cân bằng sẽ chuyển về phía làm giảm nhiệt độ (thu nhiệt).
3. đúng
4. đúng
5. sai, nồng độ thay đổi không làm thay đổi hằng số cân bằng. Hằng số cân bằng chỉ thay đổi khi thay đổi nhiệt độ.
6. sai: chỉ tính những chất khí hoặc những chất tan trong dung dịch, nếu là chất rắn thì không được tính.
=> Đáp án C

1. sai: cân bằng hóa học là cân bằng động
2. đúng: phản ứng nghịch thu nhiệt, khi tăng nhiệt độ cân bằng sẽ chuyển về phía làm giảm nhiệt độ (thu nhiệt).
3. đúng
4. đúng
5. sai, nồng độ thay đổi không làm thay đổi hằng số cân bằng. Hằng số cân bằng chỉ thay đổi khi thay đổi nhiệt độ.
6. sai: chỉ tính những chất khí hoặc những chất tan trong dung dịch, nếu là chất rắn thì không được tính.
Đáp án C
\(\Delta_rH^0_{298}=-1300kJ\) nên phản ứng là toả nhiệt.
Nhiệt lượng toả ra là 1 300 kJ nên dễ dàng thấy được phản ứng trên xảy ra thuận lợi. Hay ethanol dễ cháy, khi cháy toả nhiều nhiệt.