Người ta cho 1 mol CH3COOH tác dụng với 1 mol C3H7OH. Ở t°C, cân bằng sẽ đạt được khi có 0,6 mol este tạo thành. Theo phản ứng CH3COOH + C3H7OH => CH3COOC3H7+ H2O Nếu sau đó cho thêm 1 mol CH3COOH, thì thành phần về số mol các chất trong hỗn hợp sau khi cân bằng mới thành lập là bao nhiêu? Biết rằng hằng số tốc độ của phản ứng thuận gấp 2,25 lần hằng số tốc độ của phản ứng nghịch.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


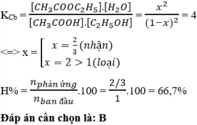
Đáp án B
TN1:
CH3COOH + C2H5OH D CH3COOC2H5 + H2O
Ban đầu: 1 1 0 0
Phản ứng:2/3 2/3 2/3 2/3
Cân bằng:1/3 1/3 2/3 2/3
Hằng số cân bằng:
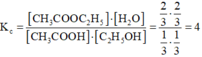
TN2:
CH3COOH + C2H5OH D CH3COOC2H5 + H2O
Ban đầu: 1 x 0 0
Phản ứng:0,9.1à0,9 0,9 0,9
Cân bằng:0,1 (x-0,9) 0,9 0,9
Hằng số cân bằng:
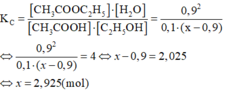

Đáp án B
TN1:
CH3COOH + C2H5OH D CH3COOC2H5 + H2O
Ban đầu: 1 1 0 0
Phản ứng:2/3 2/3 2/3 2/3
Cân bằng:1/3 1/3 2/3 2/3
Hằng số cân bằng:


Đáp án D
Giả sử phản ứng xảy ra hoàn toàn thì axit sẽ hết và ancol còn dư.
Do đó phản ứng sẽ tính theo axit.
Ở trạng thái cân bằng, đặt
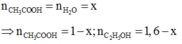

Đáp án D
Giả sử phản ứng xảy ra hoàn toàn thì axit sẽ hết và ancol còn dư.
Do đó phản ứng sẽ tính theo axit.
Ở trạng thái cân bằng, đặt n CH 3 COOH = n H 2 O = x
⇒ n CH 3 COOH = 1 - x ; n C 2 H 5 OH = 1 , 6 - x

CH3COOH(lỏng) + C2H5OH(lỏng) ↔ CH3COOC2H5(lỏng) + H2O(lỏng) .
Ban đầu: x 1
Phản ứng: 0,7 0,7 0,7 0,7
Sau: x - 0,7 0,3 0,7 0,7
Vì k = 2,25 nên:
0,7.0,7 : 0,3(x-0,7) = 2,25
=> x = 1,426 mol.
=> Đáp án B

Đáp án: B
Giả sử có 1 mol ancol , 1 mol axit , sau phản ứng tạo x mol este
=> n ancol dư = n axit dư = 1 - x
CH 3 COOH + C 2 H 5 OH → CH 3 COOC 2 H 5 + H 2 O 1 - x 1 - x x x
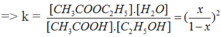
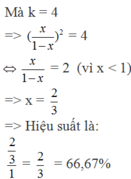

Đáp án C
Phương trình hóa học:
CH3COOH + C2H5OH D CH3COOC2H5 + H2O
Ban đầu: 1 1
Phản ứng: 2/3 2/3 2/3 2/3
Cân bằng: 1/3 1/3 2/3 2/3
Hằng số cân bằng:

Vì H = 80% (tính theo axit) nên naxit(pu) = 0,8 mol
CH3COOH + C2H5OH D CH3COOC2H5 +H2O
Ban đầu: 1 x
Phản ứng:0,8à 0,8 à 0,8 à 0,8
Cân bằng:0,2 (x-0,8) 0,8 0,8
Hằng số cân bằng:
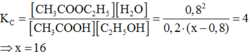

Đáp án C
Phương trình hóa học:
CH3COOH + C2H5OH D CH3COOC2H5 + H2O
Ban đầu: 1 1
Phản ứng: 2/3 2/3 2/3 2/3
Cân bằng: 1/3 1/3 2/3 2/3
Hằng số cân bằng:
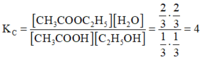
Vì H = 80% (tính theo axit) nên naxit(pu) = 0,8 mol
CH3COOH + C2H5OH D CH3COOC2H5 +H2O
Ban đầu: 1 x
Phản ứng:0,8à 0,8 à 0,8 à 0,8
Cân bằng:0,2 (x-0,8) 0,8 0,8
Hằng số cân bằng:
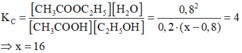
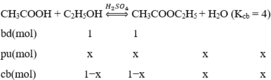
Gọi k1 là hằng số tốc độ của phản ứng thuận; k2 là hằng số tốc độ của phản ứng nghịch
\(CH_3COOH+C_3H_7OH⇌CH_3COOC_3H_7+H_2O\)
Ta có:
\(k_1=\dfrac{\left[CH_3COOC_3H_7\right]}{\left[CH_3COOH\right].\left[C_3H_7OH\right]};k_2=\dfrac{\left[CH_3COOH\right].\left[C_3H_7OH\right]}{\left[CH_3COOC_3H_7\right]}\)
Ở trạng thái cân bằng dung dịch chứa 1,4 - x (mol) CH3COOH; 1,4 - x (mol) C3H7OH và 0,6 + x (mol) CH3COOC3H7
\(\Rightarrow\dfrac{\left(0,6+x\right)}{\left(1,4-x\right).\left(1,4-x\right)}=2,25.\dfrac{\left(1,4-x\right)\left(1,4-x\right)}{0,6+x}\Rightarrow x\simeq0,53\)
Từ đó kết luận ở trạng thái cân bằng dung dịch chứa....