Câu 5: Cho m gam kim loại Al tác dụng hết với lượng vừa đủ với dung dịch HNO3, thu được dung dịch X và 0,896 lít hỗn hợp khí Y (ở đktc) gồm NO và N2O. Tỉ khối của Y so với H2 bằng 20,25. a tính giá trị của m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nHNO3 ban đầu = 1,425
MX = 32,8; Sử dụng sơ đồ đường chéo ⇒ n NO = 0,2 ; n N2O = 0,05
Ta có nNO3- trong muối kl = ne = 8nN2O + 8nNH4NO3
Bảo toàn nguyên tố N: nHNO3 ban đầu = n NO + 2n N2O + 2n NH4NO3 + n NO3- trong muối KL
⇒ nHNO3 ban đầu = 4 nNO + 10 nN2O + 10 nNH4NO3
⇒ nNH4NO3 = 0,0125
⇒ nNO3-/muối KL= 1,1
⇒ m = mNO3-/muối kl + mKL + mNH4NO3 = 1,1.62 +29 + 0,0125.80 = 98,2g
Đáp án A.

nHNO3 ban đầu = 1,425
MX = 32,8; Sử dụng sơ đồ đường chéo ⇒ n NO = 0,2 ; n N2O = 0,05
Ta có nNO3- trong muối kl = ne = 8nN2O + 8nNH4NO3
Bảo toàn nguyên tố N: nHNO3 ban đầu = n NO + 2n N2O + 2n NH4NO3 + n NO3- trong muối KL
⇒ nHNO3 ban đầu = 4 nNO + 10 nN2O + 10 nNH4NO3
⇒ nNH4NO3 = 0,0125
⇒ nNO3-/muối KL= 1,1
⇒ m = mNO3-/muối kl + mKL + mNH4NO3 = 1,1.62 +29 + 0,0125.80 = 98,2g
Đáp án A.

Đáp án A
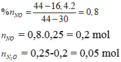
Khi Kim loại tác dụng với HNO3 ta có công thức tổng quát:


Đáp án : B
X + O2 vừa đủ => Z : NO2 ; N2O ; N2
=> khí T gồm N2O và N2 có M = 40g và n = 0,2 mol
=> nN2O = 0,15 ; nN2 = 0,05 mol
=> nNO = nX – nT = 0,1 mol
NaOH + Y => kết tủa lớn nhất gồm Mg(OH)2 và Al(OH)3
=> mkết tủa – mKL = 39,1 = mOH => nOH = 2,3 mol
Vì nAl : nMg = 5 : 4 => nAl = 0,5 ; nMg = 0,4 mol
Bảo toàn e : 2nMg + 3nAl = 3nNO + 8nN2O + 10nN2 + 8nNH4NO3
=> nNH4NO3 = 0,0375 mol
=> nHNO3 pứ = 10nNH4NO3 + 4nNO + 10nN2O + 12nN2 = 2,875 mol
Thực tế lầy dư axit 20% so với phản ứng => nHNO3 đầu = 3,45 mol
=> mdd HNO3 đầu = 1086,75g
Bảo toàn khối lượng : mKL + mdd HNO3 = mdd sau + mkhí
=> mdd sau = 1098,85g
=> C%Al(NO3)3 = 9,69%

Đáp án : D
.nX = 0,3 mol ; nZ = 0,2 mol
Chỉ có NO phản ứng với O2 tạo NO2 bị hấp thụ vào nước
=> nNO = 0,3 – 0,2 = 0,1 mol
MZ= 40g (Z gồm N2 và N2O )
=> nN2 = 0,05 mol ; nN2O = 0,15 mol
.m(g) P : Mg,Al -> Kết tủa lớn nhất : Mg(OH)2 ; Al(OH)3 : (m + 39,1)g
=> mOH = (m + 39,1) – m = 39,1g => nOH = 2,3 mol = 2nMg + 3nAl
Lại có : nMg : nAl = 4 : 5 => nMg = 0,4 mol ; nAl = 0,5 mol
Bảo toàn e : 2nMg + 3nAl = 10nN2 + 8nN2O + 3nNO + 8nNH4NO3
=> nNH4NO3 = 0,0375 mol
=> Bảo toàn N : nHNO3 pứ = 2nMg + 3nAl + 2nN2 + nNO + 2nN2O + 2nNH4NO3
=> nHNO3 pứ = 2,875 mol
=> nHNO3 đầu = 3,45 mol => mdd HNO3 = 1086,75g
=> mdd sau = mP + mdd HNO3 - mkhí = 1098,85g
=> %CAl(NO3)3 = 9,69%

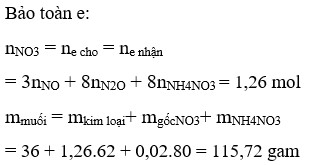
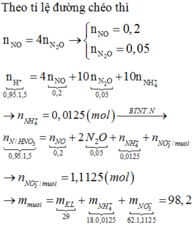

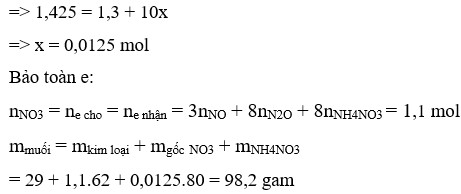

\(n_{NO}=a;n_{N_2O}=b\\ BTe:\dfrac{3m}{27}=3a+b\\ a+b=\dfrac{0,896}{22,4}=0,04mol\\ 30a+44b=0,04.20,25.2=1,62\\ \Rightarrow a=0,01;b=0,03\\ m=0,54\)