Sục 11,2l hỗn hợp(đktc) gồm khí etilen và metan vào 0,2l dung dịch brom(vừa đủ) thấy có 16g brom đã phản ứng.
a/Viết phương trình hoá học sảy ra
b/Tính thành phần % thể tích của mỗi khí trong hỗn hợp(đktc)
c/ Tính nồng độ mol của dung dịch brom đã phản ứng

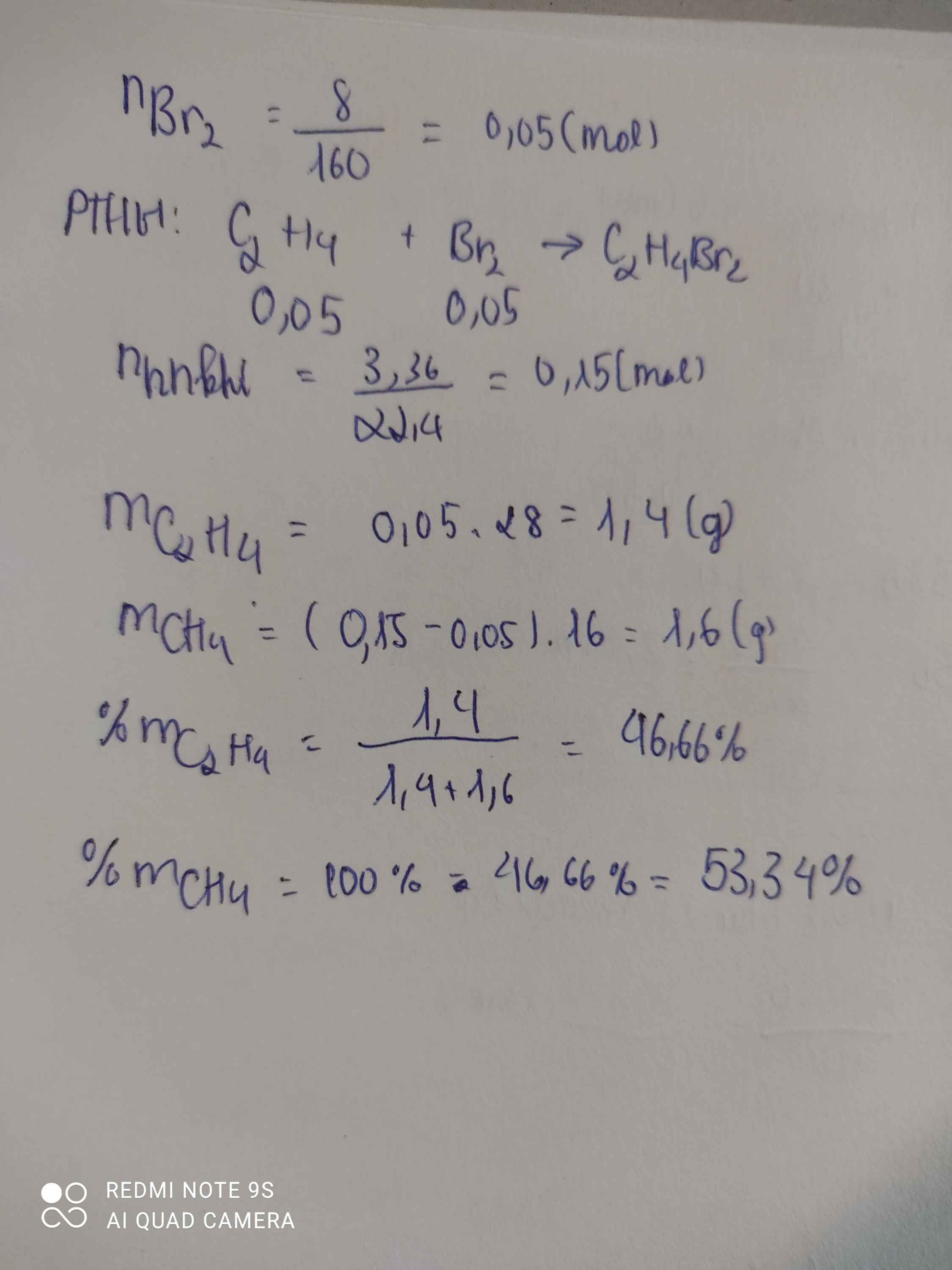
\(a/C_2H_4+Br_2\xrightarrow[]{}C_2H_4Br_2\\ b/n_{Br_2}=\dfrac{16}{160}=0,1\left(mol\right)\\ C_2H_4+Br_2\xrightarrow[]{}C_2H_4Br_2\\ \Rightarrow n_{Br_2}=n_{C_2H_4}=n_{C_2H_4Br_2}=0,1mol\\ \%V_{C_2H_4}=\dfrac{0,1.22,4}{11,2}\cdot100\%=20\%\\ \%V_{CH_4}=100\%-20\%=80\%\\ c/C_{MBr_2}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)