Bài 1. Đốt cháy hoàn toàn 13,44 lít (đktc) hỗn hợp gồm C2H2 và C2H4 thu được 18 gam nước. Xác định thành phần % thể tích của mỗi chất khí trong hỗn hợp?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi số mol C 2 H 2 và C 2 H 4 trong hỗn hợp là x, y.
Ta có x + y = 6,72/22,4 = 0,3 mol
2 C 2 H 2 + 5 O 2 → 4C O 2 + 2 H 2 O
C 2 H 4 + 3 O 2 → 2C O 2 + 2 H 2 O
Theo phương trình hoá học của phản ứng cháy, ta có :
n CO 2 = 2x + 2y => m CO 2 = 44(2x + 2y)
n H 2 O = x + 2y → m H 2 O = 18 (x + 2y)
Theo đề bài, khối lượng bình Ca OH 2 tăng lên chính là khối lượng của C O 2 và H 2 O . Vậy :
m CO 2 + m H 2 O = 44(2x + y) + 18 (x + 2y) = 33,6g
Ta có các phương trình : x + y = 0,3
106x + 124y = 33,6
Giải ra ta được : x = 0,2 ; y = 0,1.
% V C 2 H 2 = 0,2x22,4/6,72 x 100% = 66,67%
% V C 2 H 4 = 33,33%
n CO 2 = 2(x+y) = 0,6 mol = n CaCO 3
m CaCO 3 = 0,6 x 100 = 60g

a, \(CH_4+2O_2\underrightarrow{t^o}CO_2+H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Ta có: \(n_{CH_4}+n_{C_2H_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\left(1\right)\)
Theo PT: \(n_{CO_2}=n_{CH_4}+2n_{C_2H_2}=\dfrac{56}{22,4}=2,5\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,5\left(mol\right)\\n_{C_2H_2}=1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,5.22,4}{33,6}.100\%\approx33,33\%\\\%V_{C_2H_2}\approx66,67\%\end{matrix}\right.\)
b, Theo PT: \(n_{O_2}=2n_{CH_4}+\dfrac{5}{2}n_{C_2H_2}=3,5\left(mol\right)\Rightarrow m_{O_2}=3,5.32=112\left(g\right)\)

Ta có: \(n_{hhk}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{C_2H_2}=y\left(mol\right)\end{matrix}\right.\)
⇒ x + y = 0,3 (1)
Có: \(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
____x__________________2x (mol)
\(C_2H_2+\dfrac{5}{2}O_2\underrightarrow{t^o}2CO_2+H_2O\)
__y__________________y (mol)
⇒ 2x + y = 0,4 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
Ở cùng điều kiện nhiệt độ và áp suất, % thể tích cũng là % số mol.
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,1}{0,3}.100\%\approx33,33\%\\\%V_{C_2H_2}\approx66,67\%\end{matrix}\right.\)
Bạn tham khảo nhé!

Sửa:
Ta có: \(n_{hh_X}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
Gọi x, y lần lượt là số mol của CH4 và C2H2
PTHH: \(CH_4+2O_2\overset{t^o}{--->}CO_2+2H_2O\left(1\right)\)
\(C_2H_2+\dfrac{5}{2}O_2\overset{t^o}{--->}2CO_2+H_2O\left(2\right)\)
Theo PT(1): \(n_{H_2O}=2.n_{CH_4}=2x\left(mol\right)\)
Theo PT(2): \(n_{H_2O}=n_{C_2H_2}=y\left(mol\right)\)
\(\Rightarrow2x+y=0,4\) (*)
Theo đề, ta lại có: \(x+y=0,3\) (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}2x+y=0,4\\x+y=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow\%_{V_{CH_4}}=\dfrac{0,1}{0,3}.100\%=33,3\%\)
\(\%_{V_{C_2H_2}}=100\%-33,3\%=66,7\%\)
Ta có: \(n_{hh_X}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
Gọi x, y lần lượt là số mol của CH4 và C2H2
PTHH:
\(C_2H_4+3O_2--->2CO_2\uparrow+2H_2O\) (1)
\(C_2H_2+\dfrac{5}{2}O_2--->2CO_2\uparrow+H_2O\) (2)
Theo PT(1): \(n_{H_2O}=2.n_{C_2H_4}=2x\left(mol\right)\)
Theo PT(2): \(n_{H_2O}=n_{C_2H_2}=y\left(mol\right)\)
\(\Rightarrow2x+y=0,4\) (*)
Theo đề, ta lại có: \(x+y=0,3\) (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}2x+y=0,4\\x+y=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow\%_{V_{CH_4}}=\dfrac{0,1}{0,3}.100\%=33,3\%\)
\(\%_{V_{C_2H_2}}=100\%-33,3\%=66,7\%\)

\(Đặt:n_{CH_4}=a\left(mol\right),n_{C_2H_4}=b\left(mol\right)\)
\(\Rightarrow a+b=0.15\left(1\right)\)
\(n_{CO_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(CH_4+2O_2\underrightarrow{t^0}CO_2+2H_2O\)
\(C_2H_4+3O_2\underrightarrow{t^0}2CO_2+2H_2O\)
\(\Rightarrow a+2b=0.2\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.05\)
Vì : tỉ lệ thể tích tương ứng với tỉ lệ số mol :
\(\%n_{CH_4}=\dfrac{0.1}{0.15}\cdot100\%=66.67\%\)
\(\%n_{C_2H_4}=100-66.67=33.33\%\)
Chúc em học tốt !!
Đặt \(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{C_2H_4}=y\left(mol\right)\end{matrix}\right.\)
\(\Sigma n_{hhkA}=\dfrac{3,36}{22,4}=0,15\\ \rightarrow x+y=0,15\left(1\right)\)
\(PTHH:CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
(mol)........x....->...2x.......x..............2x
\(PTHH:C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
(mol)........y......->...3y...........2y........2y
\(\Sigma n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ \rightarrow x+2y=0,2\)
Giải hpt (1) (2) ta được x=0,1 ; y=0,05
\(\%V_{CH_4}=\dfrac{0,1.22,4}{3,36}.100\%=66,67\%\\ \%V_{C_2H_4}=100\%-66,67\%=33,33\%\)

\(n_{CO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
Gọi số mol C2H4, C2H2 là a, b (mol)
Bảo toàn C: 2a + 2b = 0,5
Bảo toàn H: 4a + 2b = 0,8
=> a = 0,15 (mol); b = 0,1 (mol)
\(\left\{{}\begin{matrix}\%n_{C_2H_4}=\dfrac{0,15}{0,15+0,1}.100\%=60\%\\\%n_{C_2H_2}=\dfrac{0,1}{0,15+0,1}.100\%=40\%\end{matrix}\right.\)

- Đem hiđro hóa hỗn hợp không làm thay đổi thành phần C có trong hỗn hợp.
- Vậy khí CO 2 thu được ở phần 2 bằng lượng khí thu được ở phẩn 1 và bằng 22,4 lít.
- Chọn đáp án B.

Khối lượng trung bình của 1 mol A :
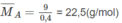
Trong hỗn hợp A phải có chất có M < 22,5 ; chất đó chỉ có thể là C H 4 .
Sau đó giải hệ 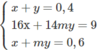
Ta tìm được m = 3; x = 0,3; y = 0,1.

Hiđro hóa không làm thay đổi C trong hỗn hợp
Áp dụng định luật bảo toàn C ⇒ V = VCO2 khi đốt cháy hỗn hợp = 4,48
Đáp án C.
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
x x
\(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
y 2y
Gọi x là số mol của C2H2 (x,y>0)
y là số mol của C2H4
Ta có : \(22,4x+22,4y=13,44\)
\(n_{H_2O}=\dfrac{18}{18}=1\left(mol\right)\)
\(n_{H_2O}=2x+y=1\) ( Theo PTHH )
Ta có hệ PT :
\(\left\{{}\begin{matrix}22,4x+22,4y=13,44\\x+2y=1\end{matrix}\right.\)
Giải hệ PT , ta có :
x = 0,2
y = 0,4
\(V_{C_2H_2}=0,2.22,4=4,48\left(l\right)\)
\(\%V_{C_2H_2}=\dfrac{4,48}{13,44}.100\%\approx33,33\%\)
\(\%V_{C_2H_4}=\dfrac{0,4.22,4}{13,44}.100\%\approx66,67\%\)