Cho 13,4 g hỗn hợp X gồm ancol etylic và axit cacboxylic mạch hở no đơn chức tác dụng với natri dư thì sinh ra 2,24 lít khí (điều kiện chuẩn). Mặt khác, cho 26,8 g hỗn hợp X tác dụng với một lượng dư dung dịch Na2CO3 thì sinh ra 3,36 lít khí (điều kiện chuẩn). a) Xác định công thức cấu tạo của axit b) Nếu đun nóng được hỗn hợp X ban đầu với H2SO4 đặc thì sau phản ứng đạt trạng thái cân bằng thu được 4,08 gam este. Tính hiệu suất của phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
- Do X tác dụng với AgNO3 sinh ra Ag
=> Trong X có một este dạng HCOOR1
- Mà cho X td với NaOH thu được 2 muối của 2 axit cacboxylic đồng đẳng kế tiếp
=> este còn lại có dạng CH3COOR2
nHCOOR1=0,5nAg=0,1 mol
=> nCH3COOR2=0,25-0,1=0,15 mol
=>Tỉ lệ mol của HCOOR1 và CH3COOR2 là 2/3
Trong 14,08 gam X:
![]()
![]()


Chọn đáp án C
Vì nAg = 0,2 < n Hỗn hợp
⇒ 1 este có dạng HCOOR với
nHCOOR = 0,1 mol
⇒ nEste còn lại = 0,15 mol.
+ Xem hỗn hợp chứa
Ta có nNaOH pứ = 5a
nHCOONa = 2a và n C H 3 C O O N a = 3 a
+ Bảo toàn khối lượng ta có:
14,08 + 5a×40
= 2a×68 + 3a×82 + 8,256
⇔ a = 0,032 mol.
⇒ Hỗn hợp ban đầu chứa
⇒ m A n c o l = 0 , 064 × ( R + 17 ) + 0 , 096 × ( R ' + 17 ) = 8 , 256
⇔ 2R + 3R' = 173.
+ Giải PT nghiệm nguyên ta có R = 43 (C3H7–) và R' = 29 ( C2H5–).
⇒ % m H C O O C 3 H 7 = 0 , 064 × 88 14 , 08 × 100 = 40 %

$C_6H_5OH + NaOH \to C_6H_5ONa + H_2O$
n phenol = n NaPH = 0,2.0,5 = 0,1(mol)
Ancol : CnH2n+1OH
$2C_6H_5OH + 2Na \to 2C_6H_5ONa + H_2$
$2C_nH_{2n+1}OH + 2Na \to 2C_nH_{2n+1}ONa + H_2$
n H2 = 3,36/22,4 = 0,15 = 1/2 n phenol + 1/2 n ancol
=> n ancol = (0,15 - 0,1.0,5).2 = 0,2(mol)
Suy ra :
0,1.94 + 0,2(14n + 18) = 18,6
<=> n = 2
Vậy CTPT của ancol C2H6O
b) 18,6 gam X chứa 0,1 mol phenol
Suy ra : 27,9 gam X chứa 27,9 . 0,1/18,6 = 0,15(mol)
C6H5OH + 3Br2 → C6H2Br3OH + 3HBr
0,15..................................0,15..................(mol)
=> m kết tủa = 0,15.331= 49,65 gam

Đáp án A
E tham gia phản ứng táng gương nên X là HCOOH (x mol) và Y là RCOOH (y mol) và Z là HCOO – Z – OOC – R (z mol)
nCO2 = 0,32 ; nH2O = 0,29 mol
=> z = nCO2 – nH2O = 0,03 mol
nAg = 2x + 2z = 0,16 => z = 0,05 mol
Bảo toàn khối lượng cho phản ứng cháy : => nCO2 = 0,335 mol
Bảo toàn O : nO = 2x + 2y + 4z = 0,26 => y = 0,02 mol
mE = 46.0,05 + 0,02(R + 45) + 0,03(Z + R + 89) = 8,58
=> 5R + 3Z = 271
Z là ancol 2 chức nên Z = 28 ; 42 ; 56 ; …
=> R = 29 và Z = 42 phù hợp
E + NaOH thu được chất rắn chứa : 0,08 mol HCOONa ; 0,05 mol C2H5COONa ; 0,02 mol NaOH dư
=> mrắn = 11,04g
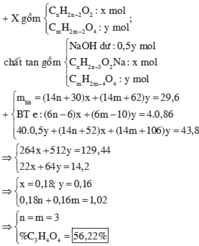


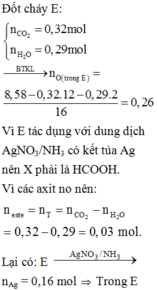

\(a,\)\(\text{Đặt axit cacboxylic là: RCOOH }\)
\(\text{nH2=}\dfrac{2,24}{22,4}=0,1mol\), \(nCO2=\dfrac{3,36}{22,4}=0,15mol\)
\(26,8gX+Na2CO3:\) 2H+ + CO32- \(->\) CO2 + H2O
\(0,3mol\) \(< -\) \(0,15mol\)
\(nRCOOHs=n\)H+=\(0,3mol\)
\(mXbđ=2mXs\) ⇒ \(nRCOOHbđ=\dfrac{nRCOOHs}{2}=0,15mol\)
\(X+Na\left(dư\right):\) \(RCOOH+Na->RCOONa+\dfrac{1}{2}H2\) \(0,15mol\) \(->\) \(0,075mol\)
\(C2H5OH+Na->C2H5ONa+\dfrac{1}{2}H2\)
\(x\)\(mol\) \(->\) \(\dfrac{1}{2}\) \(x\)\(mol\)
⇒\(nH2=0,075+\dfrac{1}{2}x\) ⇔ \(0,1=0,075+\dfrac{1}{2}x\) ⇔ \(x=0,05mol\)
\(mRCOOHbđ=mXbđ-mC2H5OH=13,4-0,05.46=11,1g\)
M\(RCOOH=\dfrac{11,1}{0,15}=74\left(đvc\right)\)⇔\(R+45=74\)⇔\(R=29\)⇒\(R\) \(\text{là}\) \(C2H5\)
\(\text{Vậy axit là}\) \(C2H5COOH\)
\(b,\)\(Xbđ->este\):\(neste=\dfrac{4,08}{102}=0,04mol\)\(C2H5COOH+C2H5OH\dfrac{H2SO4}{t0}>C2H5COOC2H5+H2O\)
\(0,04mol\) \(0,04mol\) \(< -\) \(0,04mol\)
\(\text{Vì nC2H5OOH}\)\(< \)\(\text{nC2H5COOH}\) ⇒\(\text{ %H tính theo C2H5OH}\)
\(\%H=\dfrac{nC2H5OHpu}{nC2H5OHbđ}.100\%=\dfrac{0,04}{0,05}.100\%=80\%\)