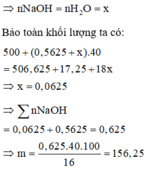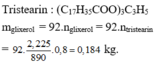Xà phòng hóa 221 kg chất béo cần dùng 120kg dung dịch NaOH thu được 228 kg xà phòng. Biết phản ứng xảy ra hoàn toàn. Nồng độ phần trăm dung dịch NaOH đã dùng là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


(![]() COO)3C3H5 + 3NaOH
COO)3C3H5 + 3NaOH
![]() 3
3![]() COONa + C3H5(OH)3
COONa + C3H5(OH)3
nglixerol = 0,2 mol
![]() nNaOH = 0,6 mol
nNaOH = 0,6 mol
![]() [NaOH] = 0,6/0,4 = 1,5M
[NaOH] = 0,6/0,4 = 1,5M
![]() Chọn C.
Chọn C.

Chọn C
( R ¯ COO)3C3H5 + 3NaOH → 3 COONa + C3H5(OH)3
nglixerol = 0,2 mol nNaOH = 0,6 mol ⇒ [NaOH] = 0,6/0,4 = 1,5M

(![]() COO)3C3H5 + 3NaOH
COO)3C3H5 + 3NaOH
![]() 3
3![]() COONa + C3H5(OH)3
COONa + C3H5(OH)3
nglixerol = 0,2 mol
nNaOH = 0,6 mol
![]() [NaOH] = 0,6/0,4 = 1,5M
[NaOH] = 0,6/0,4 = 1,5M
Chọn C.

Chọn C
( R ¯ COO)3C3H5 + 3NaOH → 3 R ¯ COONa + C3H5(OH)3
nglixerol = 0,2 mol ⇒ nNaOH = 0,6 mol ⇒ [NaOH] = 0,6/0,4 = 1,5M

Đáp án : B
Có 2 phản ứng xảy ra:
3NaOH+(RCOO)3C3H5 -> 3RCOONa+C3H5(OH)3(1)
NaOH + R'COOH -> R'COONa + H2O (2)
Ta coi các đơn vị là gam (thay vì kg)
nNaOH = 0,061 mol , nglyxerol = 0,02 mol
=> nNaOH (2) = 0,061 - 0,02.3 = 10-3
=> mH2O = 10-3 . 18 = 0,018 g
BTKL
=> 2,44 + m chất béo = 17,202 + 1,84 + 0,018
=> m chất béo = 16,62 g
<=> m chất béo = 16,62 kg (đổi lại đơn vị)

Chọn đáp án C
mKOH cần để trung hòa lương axit béo là 265,2 × 7 = 1856,4 (g)
→ nKOH = 33,15 (mol) → nNaOH cần để trung hòa lượng axit béo bằng = 33,15 (mol)
nNaOH = 213,15 (mol) → số mol NaOH tham gia phản ứng xà phòng hóa = 180 (mol)
→ nGlyxerol = 60 (mol) → mglyxerol = 5520 (g) = 5,52 (kg)

Trước hết xin nhắc lại chỉ số axit là số miligam KOH để trung hòa lượng axit béo tự do có trong 1 g chất béo.
Vậy khối lượng của KOH để trung hòa hết lượng axit béo tự do có trong 10 kg chất béo trên là:
mKOH = 7.10-3.10.1000 = 70(g) nKOH = l,25(mol)
Số mol của NaOH để trung hòa lượng axit tự do có trong 10 kg chất béo là:
nNaOH = nKOH = 1/25 (mol)
Ta lại có: nNaOH dư = nHCl = 0,5(mol); nNaOH ban đầu = 35,5(mol)


Chọn đáp án D
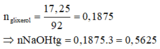
Đề bài không nói là chất béo trung tính nên ta giả sử trong chất béo có axit tự do. Gọi x là số mol axit tự do