Đốt hoàn toàn 10,4 gam kim loại X(III) cần dùng 3,36 lít O2 ở đktc. a/ Xác định tên kim loại X. b/ Khối lượng oxide thu được. c/ Nấu hòa tan hoàn toàn lượng oxide trên cần dùng bao nhiêu gam H2SO4 .
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: 4X + 3O2 --to--> 2X2O3
2/15 <- 0,1 -------> 1/15
\(M_X=\dfrac{10,4}{\dfrac{2}{15}}=78\left(\dfrac{g}{mol}\right)\)
Bạn ơi đề có bị sai ko vậy :)?

\(a.PTHH:2X+3H_2SO_4--->X_2\left(SO_4\right)_3+3H_2\uparrow\)
b. Ta có: \(n_{H_2SO_4}=\dfrac{17,64}{98}=0,18\left(mol\right)\)
Theo PT: \(n_X=\dfrac{2}{3}.n_{H_2SO_4}=\dfrac{2}{3}.0,18=0,12\left(mol\right)\)
\(\Rightarrow M_X=\dfrac{3,24}{0,12}=27\left(\dfrac{g}{mol}\right)\)
Vậy X là kim loại nhôm (Al)
\(c.PTHH:2Al+3H_2SO_4--->Al_2\left(SO_4\right)_3+3H_2\uparrow\)
Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}.n_{Al}=\dfrac{1}{2}.0,12=0,06\left(mol\right)\)
\(\Rightarrow m_{Al_2\left(SO_4\right)_3}=0,06.342=20,52\left(g\right)\)
d. Theo PT: \(n_{H_2}=n_{H_2SO_4}=0,18\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,18.22,4=4,032\left(lít\right)\)

a)
Gọi hóa trị của kim loại M là n
M + nHCl → MCln + n/2H2
nHCl = = 0,6 mol
nM = => MM = = 12n
=> Với n = 2 và MM = 24 g/mol là giá trị thỏa mãn
Kim loại M là Magie (Mg)
\(a,X+2HCl\rightarrow XCl_2+H_2\\ n_{HCl}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\\ n_X=n_{XCl_2}=n_{H_2}=\dfrac{n_{HCl}}{2}=\dfrac{0,6}{2}=0,3\left(mol\right)\\ b,M_X=\dfrac{7,2}{0,3}=24\left(\dfrac{g}{mol}\right)\\ \Rightarrow X:Magie\left(Mg=24\right)\\ c,m_{MgCl_2}=0,3.95=28,5\left(g\right)\\ d,V_{H_2\left(\text{đ}ktc\right)}=0,3.22,4=6,72\left(l\right)\)

Ta có: \(m_{HCl}=10.21,9\%=2,19\left(g\right)\Rightarrow n_{HCl}=\dfrac{2,19}{36,5}=0,06\left(mol\right)\)
Gọi CTHH của oxit là AO.
PT: \(AO+2HCl\rightarrow ACl_2+H_2O\)
Theo PT: \(n_{AO}=\dfrac{1}{2}n_{HCl}=0,03\left(mol\right)\)
\(\Rightarrow M_{AO}=\dfrac{2,4}{0,03}=80\left(g/mol\right)\)
\(\Rightarrow M_A=80-16=64\left(g/mol\right)\)
→ A là Cu.
Vậy: CTHH cần tìm là CuO.

Đáp án B
Chỉ xét kim loại trước H, nếu ko được, chọn Cu
Nhận xét: theo bảo toàn e: 2a + nb = 0,05.2 = 0,1
3a + mb = 0,045.4= 0,18 mol →như vậy m > 3 đoán ra Sn
56 a + 119 b = 4 , 69 a + b = 0 , 05 → a = 0 , 02 b = 0 , 03
%mM= 0,03.119/4,69 = 76,12%

4) x,y lần lượt là số mol của M và M2O3
=> nOxi=3y=nCO2=0,3 => y=0,1
Đề cho x=y=0,1 =>0,1M+0,1(2M+48)=21,6 =>M=56 => Fe và Fe2O3
=> m=0,1.56 + 0,1.2.56=16,8
2)X + 2HCl === XCl2 + H2
n_h2 = 0,4 => X = 9,6/0,4 = 24 (Mg)
=>V_HCl = 0,4.2/1 = 0,8 l

a) PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑
2 mol : 3 mol : 1 mol : 3 mol
0,1 mol <-- 0,15 mol <--- 0,15 mol
số mol của H2 là: 3,36 / 22,4 = 0,15 mol
khối lượng Al là: 0,1 * 27 = 2,7 g
ta có: 8 g chất rắn không tan sau phản ứng là: Cu
vậy khối lượng hỗn hợp a là: mAl + mCu = 2,7 + 8 = 10,7 g
b) khối lượng chất tan của H2SO4 là: mchất tan= 0,15 * 98 = 14,7 g
ta có: C% H2SO4= (mchất tan/ m dung dịch) * 100
→ m dung dịch H2SO4 = ( m chất tan * 100) / C% = ( 14,7 * 100) / 20= 73,5 g

R2O3+6HCl->2RCl3+3H2O
nHCl=0.3(mol)
->nR=0.05(mol)->MR2O3=8:0.05=160(g/mol)
->MR=(160-16*3):2=56(g/mol)->M là Fe
Bài 2
nH2=0.3(mol)
2X+2nHCl->2XCln+nH2(n là hóa trị của kim loại)
nX=0.6:n
+) n=1->MX=9(g/mol)->loại
+)n=2->MX=18(g/mol)->loại
+)n=3->MX=27(g/mol)->X là Al
Bài cuối bạn viết phương trình,chỉ phương trình Al+H2SO4 mới tạo khí thôi,vậy bạn tính được khối lượng nhôm,từ đó tính ra khối lượng nhôm oxit nhé,vì đang vội nên mình không giải giúp bạn được
Bài 3
nH2 = \(\frac{13,44}{22,4}\) = 0,6 mol
2Al + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2 \(\uparrow\) (1)
0,4 <---- 0,6 <-------- 0,2 <------ 0,6 (mol)
Al2O3 + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2O (2)
a) %mAl = \(\frac{0,4.27}{31,2}\) . 100% = 34,62%
%mAl2O3 = 65,38%
b) nAl2O3 = \(\frac{31,2-0,4.27}{102}\) = 0,2 (mol) = nAl2(SO4)3
Theo pt(2) nH2SO4 = 3nAl2O3 = 0,6 (mol)
m dd H2SO4 = \(\frac{\left(0,6+0,6\right)98}{20\%}\) = 588(g)
c) m dd spư = 31,2 + 588 - 0,6 . 2 = 618 (g)
C%(Al2(SO4)3) = \(\frac{\left(0,2+0,2\right)342}{618}\) . 100% = 22,14%
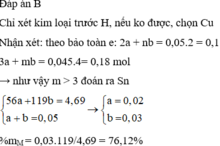
a, \(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PT: \(4X+3O_2\underrightarrow{t^o}2X_2O_3\)
Theo PT: \(n_X=\dfrac{4}{3}n_{O_2}=0,2\left(mol\right)\)
\(\Rightarrow M_X=\dfrac{10,4}{0,2}=52\left(g/mol\right)\)
→ X là Crom.
b, \(n_{Cr_2O_3}=\dfrac{1}{2}n_{Cr}=0,1\left(mol\right)\)
\(\Rightarrow m_{Cr_2O_3}=0,1.152=15,2\left(g\right)\)
c, \(Cr_2O_3+3H_2SO_4\rightarrow Cr_2\left(SO_4\right)_3+3H_2O\)
\(n_{H_2SO_4}=3n_{Cr_2O_3}=0,3\left(mol\right)\Rightarrow m_{H_2SO_4}=0,3.98=29,4\left(g\right)\)
help mik với