Dẫn 11,2 lít hỗn hợp A gồm khí metan và etilen qua bình chứa dung dịch brom dư, sau phản ứng có 4,48 lít khí thoát ra. Các khí ở đktc a) viết pt hoá học b) tính thành phần phần trăm về thể tích mỗi khí trong hỗn hợp A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a)
C2H4 + Br2 --> C2H4Br2
C2H2 + 2Br2 --> C2H2Br4
b) Gọi số mol C2H4, C2H2 là a, b (mol)
=> \(a+b=\dfrac{11,2}{22,4}=0,5\) (1)
PTHH: C2H4 + Br2 --> C2H4Br2
a---->a
C2H2 + 2Br2 --> C2H2Br4
b---->2b
=> a + 2b = \(\dfrac{112}{160}=0,7\) (2)
(1)(2) => a = 0,3 (mol); b = 0,2 (mol)
\(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,3}{0,5}.100\%=60\%\\\%V_{C_2H_2}=\dfrac{0,2}{0,5}.100\%=40\%\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{C_2H_4}=\dfrac{0,3.28}{0,3.28+0,2.26}.100\%=61,765\%\\\%m_{C_2H_2}=\dfrac{0,2.26}{0,3.28+0,2.26}.100\%=38,235\%\end{matrix}\right.\)

\(m_{Br_2}=80g\Rightarrow n_{Br_2}=0,5mol\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,5 0,5
\(n_{hh}=\dfrac{28}{22,4}=1,25mol\)
\(\Rightarrow n_{CH_4}=1,25-0,5=0,75mol\)
\(\%V_{CH_4}=\dfrac{0,75}{1,25}\cdot100\%=60\%\)
\(\%V_{C_2H_4}=100\%-60\%=40\%\)

a, \(n_{Br_2}=\dfrac{48}{160}=0,3\left(mol\right)\)
PT: \(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
_____0,15____0,3 (mol)
\(\Rightarrow\%V_{C_2H_2}=\dfrac{0,15.22,4}{11,2}.100\%=30\%\)
\(\Rightarrow\%V_{CH_4}=100-30=70\%\)
b, - Khí thoát ra ngoài là CH4.
\(V_{CH_4}=11,2.70\%=7,84\left(l\right)\)

a)
C2H4 + Br2 --> C2H4Br2
b) \(n_{Br_2}=\dfrac{32}{160}=0,2\left(mol\right)\)
PTHH: C2H4 + Br2 --> C2H4Br2
0,2<---0,2
=> \(\%V_{C_2H_4}=\dfrac{0,2.22,4}{8,96}.100\%=50\%\)
=> \(\%V_{CH_4}=100\%-50\%=50\%\)

- Đáp án A
- Khi cho hỗn hợp khí (gồm CH4 và C2H4 ) đi qua dung dịch brom thì C2H4 sẽ phản ứng hết với dung dịch brom, CH4 không tác dụng sẽ đi ra khỏi bình.
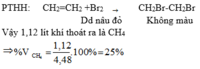

B5:
1)
\(V_{thoát}=V_{CH_4\left(đktc\right)}=3,36\left(l\right)\\ \Rightarrow\%V_{\dfrac{CH_4}{B}}=\dfrac{3,36}{4,48}.100=75\%\Rightarrow\%V_{\dfrac{C_2H_4}{B}}=100\%-75\%=25\%\)
2)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\\ CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\\ n_{CH_4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ \Rightarrow n_{CaCO_3}=n_{CO_2}=n_{CH_4}=0,15\left(mol\right)\\ \Rightarrow m_{\downarrow}=m_{CaCO_3}=100.0,15=15\left(g\right)\)

\(n_{hh.khí}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\\ n_{Br_2}=\dfrac{4}{160}=0,025\left(mol\right)\\ C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Khí metan không tác dụng với dd Br2
\(n_{C_2H_4}=n_{Br_2}=0,025\left(mol\right)\)
Vì số mol tỉ lệ thuận với thể tích. Nên:
\(\%V_{C_2H_4}=\%n_{C_2H_4}=\dfrac{0,025}{0,125}.100=20\%\\ \Rightarrow\%V_{CH_4}=100\%-20\%=80\%\)
Vậy chọn D
Chúc em học tốt và có được POP!
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(n_{Br_2}=\dfrac{4}{160}=0,025mol\)
\(V_{Br_2}=0,025.22,4=0,56l\)
\(\%V_{C_2H_4}=\dfrac{0,56.100}{2,8}=20\%\)
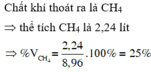
a, PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
b, - Khí thoát ra là CH4.
⇒ VCH4 = 4,48 (l)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{4,48}{11,2}.100\%=40\%\\\%V_{C_2H_4}=100-40=60\%\end{matrix}\right.\)