Một hỗn hợp X gồm MgO và Fe2O3, trong đó oxi chiếm 32,5% về khối lượng. Để hòa tan hết 3,84 gam X cần bao nhiêu ml dung dịch H2SO4 1M.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1) Số mol Ba\(\left(OH\right)_2=0,18\left(mol\right)\)
Số mol Ba\(CO_3=0,17\left(mol\right)\)
\(MgCo_3\underrightarrow{t^o}MgO+CO_2\)
\(CaCo_3\underrightarrow{t^o}CaO+CO_2\)
Ta có : 84x + 100y = 16.8 (I)
Vì \(n_{BaCO_3}\curlyvee n_{Ba\left(OH\right)_2}\)( cái đầu bn cho mũi nhọn về phái bên trái nhen ) nên bài toán xảy ra 2 trường hợp :
TH1 : Thiếu CO2 , dư Ba(OH)2
\(CO_2+Ba\left(OH\right)_2\rightarrow BaCO_3+H_2O\)
Ta có : x + y = 0,17 (II)
Từ I và II ta có hệ phương trình :
\(\left\{{}\begin{matrix}84x+100y=16,8\\x+y=0,17\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}0,0125\\0,1575\end{matrix}\right.\)
Thành phần %2 muối :
\(\%MgCO_3=6.25\%;\%CaCO_3=93.75\%\)
TH2: dư CO2 , kết của tân một phần .
( TỰ lm tiếp nhen )

Đáp án C
4,667 gam hh Na, K, Ba, ZnO trong đó %O = 5,14% + H2O → ddX + 0,032 mol H2
n O = 4 , 667 × 5 , 14 % 16 = 0 , 015 mol → nZnO = 0,015 mol.
M + nH2O → Mn+ + nOH- + 0,5nH2
nOH- = 2 x nH2 = 0,032 x 2 = 0,064 mol.
ZnO + 2OH- → ZnO22- + H2O
0,015--0,03----0,015
ddX gồm 0,034 mol OH-; 0,015 mol ZnO22-
• ddX + 0,088 mol H+
OH- + H+ → H2O
0,034--------0,034
ZnO22- + 2H+ → Zn(OH)2
0,015--------0,03
Zn(OH)2 + 2H+ → Zn2+ + 2H2O
0,012--------0,024
→ nZn(OH)2 = 0,015 - 0,012 = 0,003 mol → m↓ = 0,297 gam

Định hướng tư duy giải
Ta có:
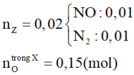
Phân chia nhiệm vụ H+:
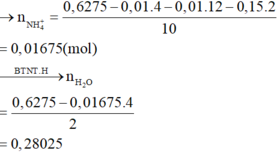
→ BTKL m = 12 , 98 + 0 , 6275 . 63 - 0 , 01 30 + 28 - 0 , 28025 . 18 = 46 , 888 .

$n_{H_2SO_4} = 0,18(mol) \Rightarrow n_{H^+} = 0,18.2 = 0,36(mol)$
$n_{H_2} = \dfrac{0,336}{22,4} = 0,015(mol)$
$2H^+ + O^{2-} \to H_2O$
$2H^+ + 2e \to H_2$
Ta có :
$n_{H^+} = 2n_O + 2n_{H_2} \Rightarrow n_O = \dfrac{0,36 - 0,015.2}{2} = 0,165(mol)$
$\Rightarrow m = m_X - m_O = 11,04 - 0,165.16 = 8,4(gam)$

Đáp án : D
nH+ = nHCl + 2nH2SO4 = 0,1 mol
Dung dịch sau có pH = 13 => COH- = 0,1M => nOH- = 0,04 mol
=> nOH (Y) = 0,14 mol = ånKL.(số điện tích)
Lại có : 2nH2 = nOH ( do các kim loại tạo ra) = 0,14 mol với 400 ml Y
=> Với 200 ml dung dịch Y có nOH tạo ra do kim loại = 0,07 mol
=> nOH tạo ra do oxit = 0,07 mol = ånKL(oxit).(số điện tích) = 2nO (bảo toàn điện tích)
=> nO = 0,035 mol
Để tạo 400 ml Y thì nO = 0,035.2 = 0,07 mol
=> m = 12,8g

Chọn B.
Dung dịch sau có pH = 13 nên sau phản ứng còn dư kiềm: nOH-dư = 0,1.0,4 = 0,04 mol.
⇒ n O H - Y = 0,04+0,2.(0,2+0,2.0,15)=0,14 mol
Quy đổi X tương đương với hỗn hợp gồm: Na (x mol), K (y mol), Ba (z mol), O (t mol).
⇒ l6t = 8,75% m.
Theo định luật bảo toàn electron, ta có: x + y + z = 2t + 2 n H 2
⇒ t = (2.0,14 - 2.0,07) : 2 = 0,07 mol ⇒ m = 12,8 ≈ 13 gam.
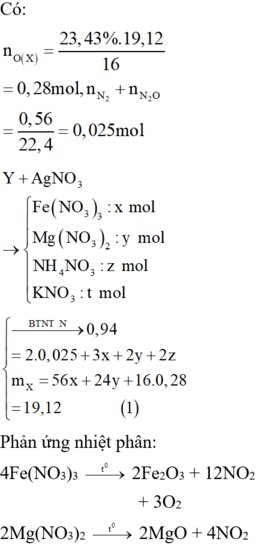
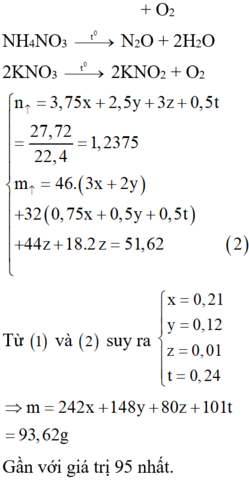

Ta có: \(40n_{MgO}+160n_{Fe_2O_3}=3,84\left(1\right)\)
Mà: Oxi chiếm 32,5% về khối lượng.
⇒ mO = 3,84.32,5% = 1,248 (g) \(\Rightarrow n_O=\dfrac{1,248}{16}=0,078\left(mol\right)\)
\(\Rightarrow n_{MgO}+3n_{Fe_2O_3}=0,078\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{MgO}=0,024\left(mol\right)\\n_{Fe_2O_3}=0,018\left(mol\right)\end{matrix}\right.\)
PT: \(MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
Theo PT: \(n_{H_2SO_4}=n_{MgO}+3n_{Fe_2O_3}=0,078\left(mol\right)\)
\(\Rightarrow V_{ddH_2SO_4}=\dfrac{0,078}{1}=0,078\left(l\right)=78\left(ml\right)\)