Khi làm lạnh 29 gam dung dịch Fe(NO3)3 41,724%, người ta thu được 8,08 gam tinh thể Fe(NO3)3.nH2O và dung dịch muối còn lại có nồng độ 34,704%. Tìm công thức tinh thể ngậm nước. 9
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Những câu hỏi liên quan

8 tháng 3 2023
Bạn xem lời giải ở đây nhé.
https://hoc24.vn/cau-hoi/hoa-tan-108-g-mg-vao-dd-h2so4-20-vua-du-sau-khi-phan-ung-ket-thuc-thu-duoc-dd-x-lam-lanh-dd-x-xuong-20-do-c-thu-duoc-1476-g-muoi-sunfat-ket-ti.4797186776937

5 tháng 9 2017
Chọn đáp án A
mFe(NO3)3 bđ = 400.12,1/100 = 48,4 (g)
Gọi số mol của Cu là x (mol)
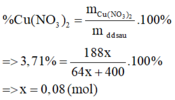
Cu + 2Fe3+ → 2Fe2+ + Cu2+
0,08 → 0,16 (mol)
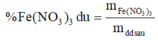
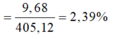
=> mFe(NO3)3 dư = 48,4 – 0,16.242 = 9,68 (g)

21 tháng 7 2019
Chọn đáp án A
mFe(NO3)3 bđ = 400.12,1/100 = 48,4 (g)
Gọi số mol của Cu là x (mol)
mdd sau = mCu + mddFe(NO3)2 => mdd sau =( 64x + 400) g
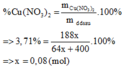
Cu + 2Fe3+ → 2Fe2+ + Cu2+
0,08 → 0,16 (mol)
=> mFe(NO3)3 dư = 48,4 – 0,16.242 = 9,68 (g)
![]()
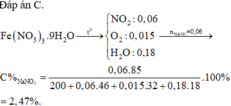
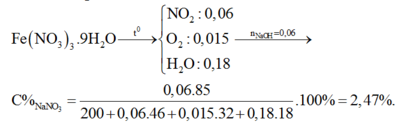


$n_{Fe(NO_3)_3} = \dfrac{29.41,724\%}{242} = 0,05(mol)$
$m_{dd\ sau\ tách\ tinh\ thể} = 29 - 8,08 = 20,92(gam)$
$n_{Fe(NO_3)_3\ sau\ tách\ tinh\ thể} = \dfrac{20,92.34,704\%}{242} = 0,03(mol)$
$\Rightarrow n_{Fe(NO_3)_3.nH_2O} = 0,05 - 0,03 = 0,02(mol)$
$\Rightarrow M_{Fe(NO_3)_3.nH_2O} = 242 + 18n = \dfrac{8,08}{0,02} = 404$
$\Rightarrow n = 9$
Vậy CT của tinh thể là $Fe(NO_3)_3.9H_2O$