Cho 25 (gam) hỗn hợp gồm Nhôm và Đồng vào dung dịch H2SO4 loãng dư, sau phản ứng thấy thoát ra 5,6 (lít) khí H2 (ở đktc). Tính khối lượng mỗi kim loại có trong hỗn hợp ban đầu.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


HD:
Thí nghiệm 1 chỉ có Na phản ứng:
Na + HOH \(\rightarrow\) NaOH + 1/2H2 (1)
0,4 0,2 mol
Thí nghiệm 2 chỉ có Al phản ứng (kim loại lưỡng tính):
Al + OH- + H2O \(\rightarrow\) AlO2- + 3/2H2 (2)
0,7/3 0,35 mol
Thí nghiệm 3 cả 3 chất đều phản ứng:
2Na + H2SO4 \(\rightarrow\) Na2SO4 + H2 (3)
Mg + H2SO4 \(\rightarrow\) MgSO4 + H2 (4)
2Al + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2 (5)
Gọi x, y, z tương ứng là số mol của Na, Mg và Al trong a gam hh.
Ta có: x = 0,4 mol; z = 0,7/3 mol; x/2 + y + 3z/2 = 0,5. Suy ra: y = -0.5 < 0 (vô lí)
Bạn xem lại đề bài, đề bài ko đúng.

a) Gọi `n_{Al} = a (mol); n_{Fe} = b (mol)`
PTHH:
`2Al + 3H_2SO_4 -> Al_2(SO_4)_3 + 3H_2`
`Fe + H_2SO_4 -> FeSO_4 + H_`
b) `n_{H_2} = (0,56)/(22,4) = 0,025 (mol)`
Theo PT: `n_{H_2} = n_{Fe} + 3/2 n_{Al}`
`=> b + 1,5a = 0,025`
Giải hpt \(\left\{{}\begin{matrix}27a+56b=0,83\\1,5a+b=0,025\end{matrix}\right.\Leftrightarrow a=b=0,01\)
=> \(\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,01.27}{0,83}.100\%=32,53\%\\\%m_{Fe}=100\%-32,53\%=67,47\%\end{matrix}\right.\)

Gọi x,y là số mol của AI và Fe
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2
x --------------------... \(\frac{3x}{2}\)
Fe + H2SO4 -> FeSO4 + H2
y ----------------------> y
n H2 = 0,56 / 22,4 = 0,025 mol
Ta có hệ \(\begin{cases}27x+56y=0,83\\x+\frac{3x}{2}=0,025\end{cases}\)
\(\begin{cases}x=0,01mol\\y=0,01mol\end{cases}\)
=> m Al = 0,01 x 27 = 0,27 g
=> m Fe = 0,01 x 56 = 0,56 g
=> % Al = 0,27 / 0,83 x 100% = 32,53 %
=> % Fe = 0,56 / 0,83 x 100% = 67,47 %

a. PTHH:
Fe + 2HCl ---> FeCl2 + H2 (1)
Mg + 2HCl ---> MgCl2 + H2 (2)
b. Gọi x, y lần lượt là số mol của Fe và Mg
Ta có: \(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Theo PT(1): \(n_{H_2}=n_{Fe}=x\left(mol\right)\)
Theo PT(2): \(n_{H_2}=n_{Mg}=y\left(mol\right)\)
\(\Rightarrow x+y=0,25\) (*)
Theo đề, ta lại có: 56x + 24y = 8,25 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}x+y=0,25\\56x+24y=8,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x\approx0,07\\y\approx0,18\end{matrix}\right.\)
=> \(m_{Fe}=0,07.56=3,92\left(g\right)\)
=> \(\%_{m_{Fe}}=\dfrac{3,92}{8,25}.100\%=47,52\%\)
\(\%_{m_{Mg}}=100\%-47,52\%=52,48\%\)

2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Fe + H2SO4 → FeSO4 + H2
nH2=\(\dfrac{8,96}{22,4}\)= 0,4 mol
Gọi số mol của Al và Fe trong 11 gam hỗn hợp là x và y mol ta có:
\(\left\{{}\begin{matrix}27x+56y=11\\1,5x+y=0,4\end{matrix}\right.\)=> x = 0,2 và y = 0,1
Theo tỉ lệ phương trình => nH2SO4 cần dùng = nH2 = 0,4 mol
=> VH2SO4 cần dùng = \(\dfrac{0,4}{2}\)= 0,2 lít
%mAl = \(\dfrac{0,2.27}{11}.100\)= 49,1% => %mFe = 100- 49,1 = 50,9%

Đáp án C
Gọi a, b là số mol của Al và Fe trong 8,3 g hỗn hợp ban đầu



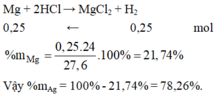
nH2 = 5.6/22.4 = 0.25 (mol)
2Al + 3H2SO4 => Al2(SO4)3 + 3H2
1/6............................................0.25
mAl = 1/6 * 27 = 4.5 (g)
mCu = 25 - 4.5 = 20.5 (g)