Cho 5,85 gam một kim loại hóa trị I tác dụng hết với nước, sau phản ứng thu được 1,68 lít khí (đktc). Tìm tên kim loại
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{H_2}=\dfrac{1,568}{22,4}=0,07\left(mol\right)\)
BT e, có: nKL = 2nH2 = 0,07.2 = 0,14 (mol)
\(\Rightarrow M_{KL}=\dfrac{3,22}{0,14}=23\left(g/mol\right)\)
Vậy: KL cần tìm là Na.

PT: \(2R+O_2\underrightarrow{t^o}2RO\)
\(n_R=\dfrac{3,6}{M_R}\left(mol\right)\)
\(n_{RO}=\dfrac{6}{M_R+16}\left(mol\right)\)
Theo PT: \(n_R=n_{RO}\Rightarrow\dfrac{3,6}{M_R}=\dfrac{6}{M_R+16}\Rightarrow M_R=24\left(g/mol\right)\)
Vậy: R là Magie.

1a)
nH2 = 2.688/22.4 = 0.12 (mol)
M + 2HCl => MCl2 + H2
0.12..............0.12......0.12
MM = 4.8/0.12 = 40
=> M là : Ca
mCaCl2 = 0.12 * 111 = 13.32 (g)

PT: \(2R+O_2\underrightarrow{t^o}2RO\)
Ta có: \(n_R=\dfrac{13}{M_R}\left(mol\right)\), \(n_{RO}=\dfrac{16,2}{M_R+16}\left(mol\right)\)
Theo PT: \(n_R=n_{RO}\Rightarrow\dfrac{13}{M_R}=\dfrac{16,2}{M_R+16}\Rightarrow M_R=65\left(g/mol\right)\)
→ R là Kẽm (Zn).

Cho 11,2g kim loại R hóa trị II tác dụng hết trong dung dịch axit sunfuric (H2SO4), sau phản ứng thu được 4,48 lít khí hiđro (đktc). Tên của kim loại R là:
A. Sắt. B. Magie. C. Niken. D. Kẽm.
Giai chi tiet :
nH2 = 4,48 : 22,4 = 0,2 (mol)
pthh : R + 2HCl --> RCl2 + H2
0,2 <--------------------- 0,2 (mol )
=> MR= 11,2 : 0,2 = 56 (g/mol)
=> R : Fe

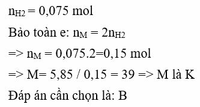
Gọi kim loại cần tìm là R
PTHH: \(R+H_2O\rightarrow ROH+\dfrac{1}{2}H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\) \(\Rightarrow n_R=0,15\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{5,85}{0,15}=39\left(đvC\right)\) \(\Rightarrow\) R là Kali
\(n_{H_2}=\dfrac{1.68}{22.4}=0,075\left(mol\right)\)
\(n_X=\dfrac{5,85}{X}\left(mol\right)\)
\(2X+2H_2O\rightarrow2XOH+H_2\uparrow\)
0,15 ←0,075
Ta có:
\(\dfrac{5,85}{X}=0,15\)
\(\Leftrightarrow X=\dfrac{5,85}{0,15}=39\left(K\right)\)
Vậy kim loại đó là K