Cho 5,6 lít hỗn hợp gồm CH4, C2H4 vào dung dịch brom. Phản ứng kết thúc thu được 18,8g đibrom etan. a. Tính thể tích mỗi khí trong hỗn hợp b. Khối lượng brom đã dùng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Ta có: \(n_{C_2H_4Br_2}=\dfrac{28,2}{188}=0,15\left(mol\right)\)
Theo PT: \(n_{C_2H_4}=n_{Br_2}=n_{C_2H_4Br_2}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,15.22,4}{5,6}.100\%=60\%\\\%V_{CH_4}=40\%\end{matrix}\right.\)
\(m_{Br_2}=0,15.160=24\left(g\right)\)

ta có :
nBr2=\(\dfrac{16}{160}=0,1mol\)
C2H4+Br2->C2H4Br2
0,1------0,1
=>VC2H4=0,1.22,4=2,24l
=>VCH4=3,36l->n CH4=0,15 mol
->%VC2H4=\(\dfrac{2,24}{5,6}.100\)=40%
=>%VCH4=60%
c)
CH4+2O2-to>CO2+2H2O
0,15---------------0,15
C2H4+3O2--to>2CO2+2H2O
0,1--------------------0,2
=>m CaCO3=0,35.100=35g

\(Gọi : n_{C_2H_4} = a; n_{C_2H_2} = b\\ \Rightarrow a + b = \dfrac{5,6}{22,4} = 0,25(1)\\ C_2H_4 + Br_2 \to C_2H_4Br_2\\ C_2H_2 + 2Br_2 \to C_2H_2Br_4\\ n_{Br_2} = a + 2b = \dfrac{56}{160} =0,35(2)\\ (1)(2)\Rightarrow a = 0,15 ; b = 0,1\\ \Rightarrow \%V_{C_2H_4} = \dfrac{0,15}{0,25} .100\% = 60\%\\ \%V_{C_2H_2} = 100\% -60\% = 40\%\)

a) Các phương trình phản ứng:
C2H4 + Br2 → C2H4Br2
C2H2 + 2Br2 → C2H2Br4
C2H2 + Ag2O → C2Ag2 + H2O
Hay
C2H2 + 2AgNO3 + 2NH3 → C2Ag2 + 2NH4NO3
b) Gọi a, b, c lần lượt là số mol của CH4, C2H4, C2H2 trong 4,3gam hỗn hợp T.
– Số mol Br2 = 0,15 (mol); số mol kết tủa = số mol C2H2 = 0,075 (mol); số mol T = 0,3 (mol). Do đó nT = 4nC2H2
– Ta có hệ phương trình:
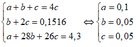
– Suy ra % thể tích mỗi khí trong T:
%VCH4 = 50%; %VC2H2 = %VC2H4 = 25%

a.\(m_{dd.Br_2\left(tăng\right)}=m_{C_2H_2}=2,6g\)
\(n_{hh}=\dfrac{5,6}{22,4}=0,25mol\)
\(n_{C_2H_2}=\dfrac{2,6}{26}=0,1mol\)
\(\%V_{C_2H_2}=\dfrac{0,1}{0,25}.100=40\%\)
\(\%V_{CH_4}=100\%-40\%=60\%\)
b.\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
0,1 0,2 ( mol )
\(C_{M\left(dd.Br_2\right)}=\dfrac{0,2}{0,1}=2M\)

1. \(n_{Br_2}=0,4.0,5=0,2\left(mol\right)\)
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Theo PT: \(n_{C_2H_4}=n_{Br_2}=0,2\left(mol\right)\Rightarrow V_{C_2H_4}=0,2.22,4=4,48\left(l\right)\)
2. \(n_{C_2H_4Br_2}=\dfrac{9,4}{188}=0,05\left(mol\right)\)
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Theo PT: \(n_{C_2H_4}=n_{C_2H_4Br_2}=0,05\left(mol\right)\)
\(\Rightarrow\%V_{C_2H_4}=\dfrac{0,05.22,4}{1,4}.100\%=80\%\)
\(\Rightarrow\%V_{CH_4}=100-80=20\%\)
\(a) C_2H_4 + Br_2 \to C_2H_4Br_2\\ n_{C_2H_4} = n_{Br_2} = n_{C_2H_4Br_2} = \dfrac{18,8}{188} = 0,1(mol)\\ V_{C_2H_4} = 0,1.22,4 = 2,24(lít)\\ V_{CH_4} = 5,6 -2,24 = 3,36(lít)\\ b) m_{Br_2} = 0,1.180 = 18(gam) \)