Cho 100(ml) dd H2SO4 0,05M và Al2(SO4)3 1M vào V(ml) dd NaOH 1M. Kết thúc thu được 3,9 g kết tủa. Tính giá trị lớn nhất của V ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Có n Al3+ = 0,1 mol
Khi thổi CO2 đến dư thì: AlO2- + CO2 + 2H2O → Al(OH)3 + HCO3-
=> n AlO2- = n kết tủa = 0,03 mol
Vậy chứng tỏ có tạo kết tủa nhưng sau đó kết tủa tan 1 phần
=> n kết tủa = n Al3+ - n AlO2- = 0,07 mol
=> n NaOH = 4n Al3+ - n kết tủa= 0,33 mol
=> V= 0,33 l
=>B

\(n_{Al2\left(SO4\right)3}=0,1\left(mol\right)\)
\(n_{Al\left(OH\right)3}=0,04\left(mol\right)\)
\(V_{max}\Leftrightarrow Al\left(OH\right)_3\) tan một phần
\(Al_2\left(SO_4\right)_3+6NaOH\rightarrow2Al\left(OH\right)_3+3Na_2SO_4\)
0,1__________0,6__________0,2___________
\(\Rightarrow\) Có 0,2-0,04 =0,16(mol) Al(OH)3 tan
\(Al\left(OH\right)_3+NaOH\rightarrow NaAlO_2+2H_2O\)
0,16_________0,16____________
\(\Sigma n_{NaOH}=0,76\left(mol\right)\)
\(\Rightarrow V=0,76\left(l\right)=760\left(ml\right)\)
Vậy đáp án đúng :D
• 0,01 mol Al2(SO4)3 + V ml NaOH → ↓
Nung ↓ → 0,03 mol Al2O3
→ nAl(OH)3 = 0,03 × 2 = 0,06 mol.
• TH1: NaOH thiếu
AlCl3 + 3NaOH → Al(OH)3↓ + 3NaCl
nNaOH = 3 × nAl(OH)3 = 3 × 0,06 = 0,18 mol → VNaOH = 0,18 : 0,1 = 1,8 lít = 1800ml.
• TH2: NaOH dư
Al2(SO4)3 + 6NaOH → 2Al(OH)3↓ + 3Na2SO4(*)
Al(OH)3 + NaOH → NaAlO2 + 2H2O (**)
==> bạn tự làm tiếp nha

Chọn đáp án C
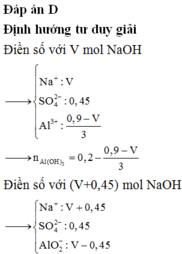
● Gọi số mol NaOH dùng ở lần 1 là a mol ta có sơ đồ.
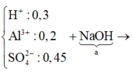
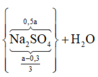
● ⇒ Với nNaOH = (a + 0,45) mol thì nAl(OH)3 = a - 0 , 3 6
+ Ta có sơ đồ:

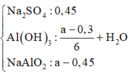
⇒ Ta có nAl(OH)3 = 4nAl(OH)3 – (nNaOH – nH+)
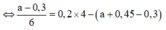
a = 0,6 mol ⇒ VNaOH = 0,6 lít = 600 ml ⇒ Chọn C
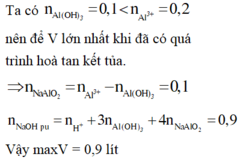
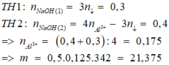


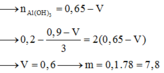
Al2(SO4)3 +6NaOH---->2Al(OH)3 +3Na2SO4(1)
Al(OH)3 +NaOH----->NaAlO2 +2H2O(2)
Ta có
nAl2(SO4)3=0,05.0,1=0,005(mol)Al2(SO4)3=0,05.0,1=0,005(mol)
Theo pthh1
nAl(OH)3=2nAl2(SO4)3=0,01(mol)Al(OH)3=2nAl2(SO4)3=0,01(mol)
Mà nAl(OH)3=0,7878=0,01(mol)Al(OH)3=0,7878=0,01(mol)
=> NaOH dư
Theo pthh
nNaOH=6nAl2(SO4)3=0,06(mol)NaOH=6nAl2(SO4)3=0,06(mol)
VNaOH=0,060,2=0,3(M)
cam on a