Bài 1: Hòa tan hết 26 gam K ẽm (Zn) vào dung d ịch axit Clohidric (HCl) thì thu dugc mu tilde o i kẽm clorua .ZnCl 2 và khí hidro a) Tinh th ể tích Hidrô tạo thành? (đktc) b) Nếu dùng lượng khí Hidrô sinh ra ở phản ứng trên để khử đồng (II) oxit (CuO) thì thu được bao nhiêu gam đồng? (Cu) ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Lập công thức hóa học của muối kẽm clorua: Z n C l 2
b) Khối lượng muối Z n C l 2 = 6,5 + 7,3 – 0,2 = 13,6 (gam)

`Zn + 2HCl -> ZnCl_2 + H_2`
`0,1` `0,2` `0,1` `(mol)`
`n_[Zn]=[6,5]/65=0,1(mol)`
`a)V_[H_2]=0,1.22,4=2,24(l)`
`b)C%_[HCl]=[0,2.36,5]/200 . 100 =3,65%`
`Zn + HCl -> ZnCl_2 + H_2` `\uparrow`
`n_(Zn) = (6,5)/65 = 0,1 mol`.
`n_(H_2) = 0,1 mol`.
`V(H_2) = 0,1 xx 22,4 = 2,24l`.
`C%(HCl) = (0,2.36,5)/200 xx 100 = 36,5%`.

a/ PTHH chữ:
kẽm + axit clohiđric ===> kẽm clorua + hidro
b/PTHH: Zn + 2HCl ===> ZnCl2 + H2
c/ Áp dụng định luật bảo toàn khối lượng, ta có
mH2 = mZn + mHCl - mZnCl2
<=> mH2 = 6,5 + 7,2 -13 = 0,7 gam
a) PT chữ:
Kẽm + Axit clohiđric -> Kẽm Clorua + Khí Hiđro

a. \(n_{Zn}=\dfrac{6.5}{65}=0,1\left(mol\right)\)
PTHH : Zn + 2HCl -> ZnCl2 + H2
0,1 0,2 0,1
b. \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c. \(m_{HCl}=0,2.36,5=7,3\left(g\right)\)
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
\(m_{HCl}=0,2\cdot36,5=7,3g\)

\(n_{Zn}=\dfrac{3,25}{65}=0,05mol\)
a)\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,05 0,1 0,05 0,05
b)\(m_{ZnCl_2}=0,05\cdot136=6,8g\)
c)\(V_{H_2}=0,05\cdot22,4=1,12l\)

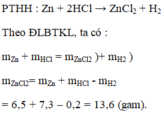
\(n_{Zn}=\dfrac{26}{65}=0,4\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,4--->0,8------>0,4------>0,4 (mol)
\(V_{H_2}=0,4.22,4=8,96\left(l\right)\)
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
0,4-->0,4 (mol)
=> \(m_{Cu}=0,4.64=25,6\left(g\right)\)