
giup mik voi
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



a: Xét ΔBAE và ΔBDE có
BA=BD
\(\widehat{ABE}=\widehat{DBE}\)
BE chung
Do đó: ΔBAE=ΔBDE
b: Ta có: ΔBAE=ΔBDE
nên \(\widehat{BAE}=\widehat{BDE}=90^0\)
hay ED\(\perp\)BC
c: Xét ΔAKE vuông tại A và ΔDCE vuông tại D có
EA=ED
\(\widehat{AEK}=\widehat{DEC}\)
Do đó: ΔAKE=ΔDCE
Suy ra: EK=EC
hay ΔEKC cân tại E



`1
a)28 là bội của 7
b)14 là ước của 28
b)2 là ước của 28
c)0 là bội của 28
2)
42 ⋮ 7
42 ko cia hết cho 8
48 ko chia hết cho 15
48⋮ 16
3
trong 1 tổng,nếu mọi số hạng chia hết cho cùng 1 số thì tổng chia hết cho số đó
nếu trong 1 tổng chỉ có đúng 1 số ko chia cho một số,các số hạng còn lại đều chia hết cho số đó thì tổng ko chia hết cho số đó
4
a) Đ b) Đ
c) S d) Đ
5 D


Part 1:
1. handkerchief
2. show your appreciation
3. a business card
4. business people
5. twice - one


 giup mik voi mik cam on!
giup mik voi mik cam on!
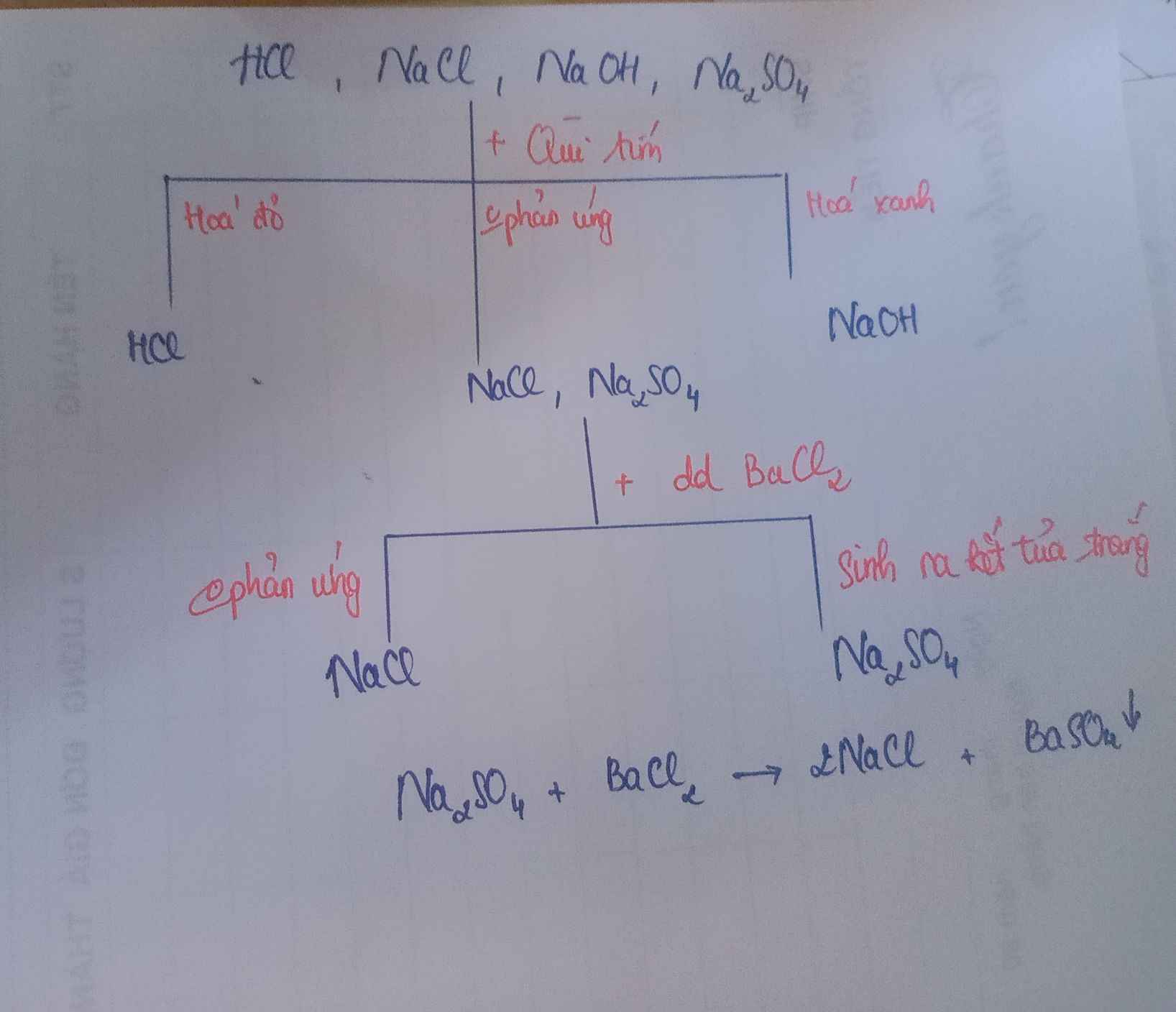

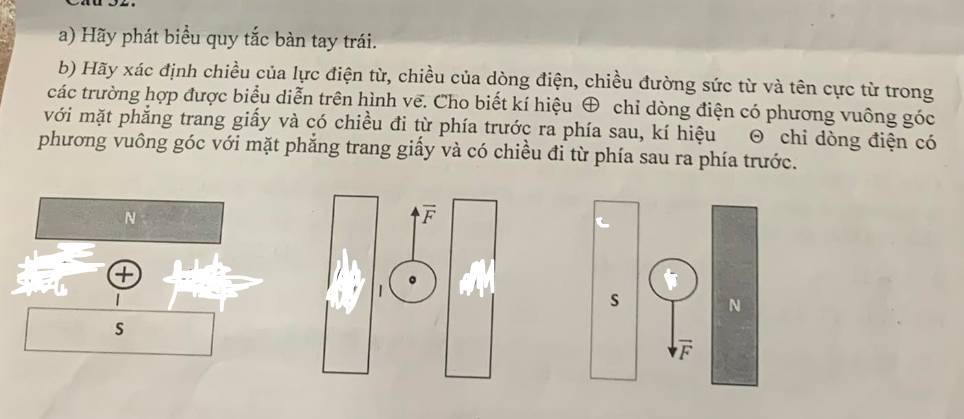



1
\(n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\\ pthh:2Mg+O_2\underrightarrow{t^o}2MgO\\ \)
0,25 0,125
\(V_{O_2}=0,125.22,4=2,8\left(l\right)\\ V_{KK}=2,8.5=14\left(l\right)\)
2
\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\\ pthh:Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
0,15 0,15 0,15
\(V_{H_2}=0,15.22,4=3,36\left(l\right)\\ m_{FeCl_2}=127.0,15=19,05\left(g\right)\\ pthh:2H_2+O_2\underrightarrow{t^o}2H_2O\)
0,15 0,15
\(m_{H_2O}=0,15.18=2,7\left(g\right)\)
\(3\\ n_{Zn}=\dfrac{26}{65}=0,4\left(mol\right)\\ n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\\ pthh:Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\\ LTL:\dfrac{0,4}{1}< \dfrac{0,5}{1}\)
=> H2SO4 dư
\(n_{H_2SO_4\left(p\text{ư}\right)}=n_{Zn}=0,4\left(mol\right)\\ m_{H_2SO_4\left(d\right)}=\left(0,5-0,4\right).98=9,8\left(g\right)\)
\(n_{ZnSO_4}=n_{Zn}=0,4\left(mol\right)\\ m_{ZnSO_{\text{ 4}}}=0,4.136=161=64,4\left(g\right)\)
dung dịch làm Qùy tím không chuyển màu vì ZnSO4 là muối
4
\(n_{Na}=\dfrac{13,8}{23}=0,6\left(mol\right)\\ pthh:Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\uparrow\)
0,6 0,6 0,3
\(m_{\text{dd}}=13,8+300-\left(0,3.2\right)=313,2\left(g\right)\\ C\%_{NaOH}=\dfrac{0,6.40}{313,2}.100\%=7,66\%\)
5
\(n_{CaO}=\dfrac{2,24}{56}=0,04\left(mol\right)\\ pthh:CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
0,04 0,04
\(m_{\text{dd}}=2,24+87,76=90\left(g\right)\\ C\%_{Ca\left(OH\right)_2}=\dfrac{0,04.74}{90}.100\%=3,289\%\)