Cho hỗn hợp gồm MgCO3 và FeCO3 vào 300 gam dung dịch HCl `7,3%`. Sau khi phản ứng kết thúc, thu được 4,48 lít khí X ở điều kiện tiêu chuẩn và dung dịch Y. Thêm từ từ dung dịch NaOH 1M vào Y đến khi kết tủa lớn nhất thấy hết V ml. Lọc lấy kết tủa đem nung ngoài không khí tới khối lượng không đổi được 11,2 gam chất rắn E. Các phản ứng hóa học xảy ra hoàn toàn, lượng HCl bay hơi không đáng kể.
a) Tính khối lượng hỗn hợp MgCO3 và FeCO3
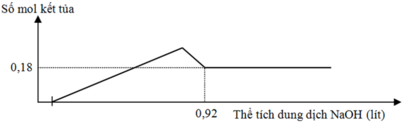
b) Tính V
c) Dẫn toàn bộ lượng khí X hấp thụ hết vào 200ml dung dịch KOH 1M và Ba(OH)2 xM thì thu được lượng lớn nhất. Tìm giá trị nhỏ nhất của x.



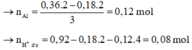
MgCO3+2HCl→MgCl2+CO2+H2O
FeCO3+2HCl→FeCl2+CO2+H2O
2NaOH+MgCl2→2NaCl+Mg(OH)2
2NaOH+FeCl2→2NaCl+Fe(OH)2
Mg(OH)2to→MgO+H2O
4Fe(OH)2+O2to→2Fe2O3+4H2O
nHCl=0,6(mol)
nCO2=0,2(mol)
Ta có:
HCl dư, CO2 hết
nHCl=0,6−0,2=0,4(mol)
NaOH+HCl→NaCl+H2O
nMgCO3=a(mol)
nFeCO3=b(mol)
nHCl=2a+2b=0,4(1)
mE=40a+80b=11,2(2)
(1)(2)
a=0,12
b=0,08
a/a/
mMgCO3=0,12.84=10,08(g)
mFeCO3=0,08.116=9,28(g)
b/
VNaOH=\(\dfrac{0,12.2+0,08.2+0,2}{1}\)=0,24(l)
c/
Ba(OH)2+CO2→BaCO3+H2O
nBa(OH)2=0,2(mol)
CMBa(OH)2=\(\dfrac{0,2}{0,2}\)=1M