Đốt cháy hoàn toàn 18.4g một hợp chất hữu cơ A. Phản ứng kết thúc ta thu được 17,92l CO2(đktc) và 21,6g H2O 1.Tính khối lượng khí O2 đã tham gia phản ứng 2.Hợp chất A chứa những n.tố hóa học nào 3.xác định công thức hóa học của A. Biết tỉ khối hơi của A so với khí Oxi bằng 1,4375 lần 4. Tính số nguyên tử có trong 18,4g A Mình cảm ơn ạ☺️
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Gọi số mol C2H4, C3H6 là a, b (mol)
=> \(a+b=\dfrac{3,36}{22,4}=0,15\left(mol\right)\) (1)
\(n_{CO_2}=\dfrac{17,6}{44}=0,4\left(mol\right)\)
PTHH: C2H4 + 3O2 --to--> 2CO2 + 2H2O
a----->3a--------->2a
2C3H6 + 9O2 --to--> 6CO2 + 6H2O
b------>4,5b------->3b
=> 2a + 3b = 0,4 (2)
(1)(2) =>a = 0,05 (mol); b = 0,1 (mol)
\(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,05}{0,15}.100\%=33,33\%\\\%V_{C_3H_6}=\dfrac{0,1}{0,15}.100\%=66,67\%\end{matrix}\right.\)
b) nO2 = 3a + 4,5b = 0,6 (mol)
=> VO2 = 0,6.22,4 = 13,44 (l)
Gọi a (mol) và b (mol) lần lượt là số mol của C2H4 và C3H6, ta có:
Giả thiết: a+b=3,36/22,4=0,15 (1).
BT C: 2a+3b=17,6/44=0,4 (2).
Giải hệ phương trình gồm (1) và (2), ta suy ra a=0,05 (mol) và b=0,1 (mol).
a. %V\(C_2H_4\)=0,05/0,15.100%\(\approx\)33,33% \(\Rightarrow\) %V\(C_3H_6\)\(\approx\)100%-33,33%\(\approx\)66,67%.
b. nnước=0,5.(0,05.4+0,1.6)=0,4 (mol).
BTKL: m\(O_2\)=17,6+0,4.18-(0,05.28+0,1.42)=19,2 (g) \(\Rightarrow\) n\(O_2\)=19,2/32=0,6 (mol).
Thể tích cần tìm là 0,6.22,4=13,44 (lít).

a) \(n_{CO_2}=\dfrac{17,6}{44}=0,4\left(mol\right)\)
=> nC = 0,4 (mol)
\(n_{H_2O}=\dfrac{10,8}{18}=0,6\left(mol\right)\)
=> nH = 1,2 (mol)
mA = mC + mH = 0,4.12 + 1,2 = 6 (g)
b)
Bảo toàn O: \(n_{O_2}=\dfrac{0,4.2+0,6}{2}=0,7\left(mol\right)\)
=> mO2 = 0,7.32 = 22,4 (g)
Sao từ số mol của CO2 mà bạn tính ra đc số mol của C vậy??

n C O 2 = 13,2 44 = 0,3 m o l → n C = 0,3 m o l ; m C = 3,6 g a m . n H 2 O = 5,4 18 = 0,3 m o l → n H = 0,6 m o l ; m H = 0,6 g a m .


Vậy A có công thức đơn giản nhất là C H 2 O n .
Lại có M A = 15 . 4 = 60 ( g / m o l ) → n = 2 thỏa mãn.
A là C 2 H 4 O 2 .
⇒ Chọn B.

Gọi CTĐGN của A là \(C_xH_y\)
\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\Rightarrow m_C=0,2\cdot12=2,4g\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3mol\Rightarrow n_H=2n_{H_2O}=0,6mol\Rightarrow m_H=0,6g\)
\(\Rightarrow x:y=n_C:n_H=0,2:0,6=1:3\)
\(\Rightarrow\left\{{}\begin{matrix}x=1\\y=3\end{matrix}\right.\)\(\Rightarrow CTĐGN\) là \(CH_3\)
Gọi CTHH cần tìm là \(\left(CH_3\right)_n\)
Theo bài: \(M_A=15\cdot2=30g\)\(\Rightarrow15n=30\Rightarrow n=2\)
Vậy A cần tìm có CTHH là \(C_2H_6\)

\(n_{CO_2}=\dfrac{4,4}{44}=0,1\left(mol\right)=n_C;n_H=2n_{H_2O}=2.\dfrac{1,8}{18}=0,2\left(mol\right)\)
\(\Rightarrow m_C=0,1.12=1,2\left(g\right);m_H=0,2.1=0,2\left(g\right)\Rightarrow m_O=3-1,2-0,2=1,6\left(g\right)\)
\(\Rightarrow n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\Rightarrow x:y:z=0,1:0,2:0,1=1:2:1\Rightarrow\left(CH_2O\right)_n\)
\(n\left(12+2+16\right)=30.2=60\Rightarrow n=2\Rightarrow C_2H_4O_2\)
BTNT oxi: \(2.n_{CO_2}+n_{H_2O}=0,1+n_{O< trong-khong-khi>}\Rightarrow n_O=0,2\left(mol\right)\)
Nhớ ko nhầm thì oxi chiếm 20% thể tích ko khí thì phải
\(\Rightarrow V_{kk}=\dfrac{22,4.0,2}{0,2}=22,4\left(l\right)\)
Ơ mà hình như nhầm chỗ Vkk rồi. Phải là bằng 22,4.0,1/0,2 mới đúng. Đây là phân tử oxi chứ ko phải nguyên tố nữa

2
nCO2 = 6,72/22,4=0,3 mol
=> nC = 0,3 mol
nH2O= 7,2/18=0,4 mol
=> nH= 0,4.2=0,8 mol
=> nC : nH = 0,3 : 0,8 = 3 : 8
=> CTĐG của hợp chất hữu cơ là (C3H8)n
Ta có: M CxHy= 1,517 x 29 = 44 (g/mol)
=>. 44n = 44 => n=1
CTHH của hợp chất hữu cơ là C3H8

a, Ta có: \(n_{CO_2}=\dfrac{17,6}{44}=0,4\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\Rightarrow n_H=0,2.2=0,4\left(mol\right)\)
⇒ mC + mH = 0,4.12 + 0,4.1 = 5,2 (g) = mA
Vậy: A chỉ chứa C và H.
Gọi CTPT của A là CxHy.
⇒ x:y = 0,4:0,4 = 1:1
→ CTPT của A có dạng là (CH)n.
Mà: \(M_A=1,625.16=26\left(g/mol\right)\)
\(\Rightarrow n=\dfrac{26}{12+1}=2\)
Vậy: CTPT của A là C2H2.
b, CTCT: \(CH\equiv CH\)
- Tchh đặc trưng: tham gia pư cộng, pư thế ion kim loại.
- Điều chế: \(2CH_4\underrightarrow{1500^o}C_2H_2+3H_2\)
\(CaC_2+2H_2O\rightarrow Ca\left(OH\right)_2+C_2H_2\)

Đáp án B
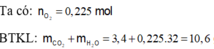
Ta có tỉ lệ số mol CO2 : H2O là 2:1, giải được số mol CO2 và H2O lần lượt là 0,2 và 0,1 mol
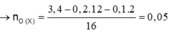
Trong X: C:H:O=4:4:1 nên X có CTPT dạng (C4H4O)n.
Do phân tử khối của X nhỏ hơn 150 thỏa mãn X là C8H8O2.
1 mol X phản ứng vừa hết 2 mol NaOH nên thỏa mãn các CTCT của X là.
CH3COOC6H5, CH2=CH-C6H3(OH)2 (có 6 đồng phân).
Vậy có thất cả 7 đồng phân của X.
\(n_{CO_2}=\dfrac{17,92}{22,4}=0,8mol\Rightarrow n_C=0,8mol\Rightarrow m_C=9,6g\)
\(n_{H_2O}=\dfrac{21,6}{18}=1,2g\Rightarrow n_H=2n_{H_2O}=2\cdot1,2=2,4mol\Rightarrow m_H=2,4g\)
\(\Rightarrow m_C+m_H=12g< m_A=18,4g\Rightarrow\)chứa O.
\(\Rightarrow m_O=18,4-12=6,4g\)
Gọi CTĐGN là \(C_xH_yO_z\)
\(x:y:z=\dfrac{m_C}{12}:\dfrac{m_H}{1}:\dfrac{m_O}{16}=\dfrac{9,6}{12}:\dfrac{2,4}{1}:\dfrac{6,4}{16}=2:6:1\)
\(\Rightarrow CTĐGN:C_2H_6O\)
a)\(C_2H_6O_2+\dfrac{5}{2}O_2\underrightarrow{t^o}2CO_2+3H_2O\)
1 0,8 1,2
\(m_{O_2}=1\cdot32=32g\)
b)Gọi CTPT là \(\left(C_2H_6O\right)_n\)
Theo bài: \(M_A=1,4375\cdot32=46\)
\(\Rightarrow46n=46\Rightarrow n=1\)
Vậy CTPT là \(C_2H_6O\)