Cho 6,72 lít khí H2 đi qua ống đựng 32g CuO nung nóng thu đc chất rắn A. Thể tích dd H2SO4 loãng 1M đủ để tác dụng hết vs A là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) 3,6 g
m=1,97(g)
VCO==20%
VCO2=20%
VH2=60%
Giải thích các bước giải:
2H2O+C->CO2+2H2
H2O+C->CO+H2
A: CO (y mol) H2(2x+y mol) CO2(x mol)+Ba(OH)2=>nkt BaCO3 x mol
CO (y mol) H2 (2x+y mol)+FeO->CO2 +B
B+H2SO4=>nSO2=0,065mol mà nH2SO4 phản ứng=0,14
=>B có oxi=>nO=0,14-0,13=0,01mol
nFe=(0,065x2+0,01x2)/3=0,05mol
=>mFeO=0,05x72=3,6g
CO2+Ca(OH)2->CaCO3 0,01mol
nCO2=0,01=>y=0,01
mặt khác y+2x+y=0,05-0,01=>x=0,01mol
m=197x0,01=1,97(g)
nhh=0,01+0,03+0,01=0,05(mol)
VCO=0,01/0,05x100=20%
VCO2=0,01/0,05x100=20%
VH2=60%
nguồn mạng nha.
\(n_{SO2}=\dfrac{1,456}{22,4}=0.065\left(mol\right);n_{CaCO_3}=\dfrac{1}{100}=0,01\left(mol\right)\)
Ta có : PTHH
\(2Fe+6H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
Thấy \(n_{H_2SO_4}:n_{SO_2}=\dfrac{0,14}{6}>\dfrac{0,065}{3}\Rightarrow\) chất rắn B có FeO dư
PTHH \(2FeO+4H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+SO_2+4H_2O\)
Đặt số mol Fe và FeOdư lần lượt là a và b (a,b>0)
có \(\left\{{}\begin{matrix}3a+2b=0,14\\1,5a+0,5b=0,065\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,04\\b=0,01\end{matrix}\right.\)
\(\Rightarrow\sum n_{FeO}=n_{Fe}+n_{FeOdu}=0,05\left(mol\right)\) (bảo toàn nguyên tố Fe)
\(\Rightarrow m_{FeO}=0,05\times56=2,8\left(g\right)\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\) \(\Rightarrow n_{CO_2}=n_{CaCO_3}=0,01\left(mol\right)\)
\(FeO+CO\rightarrow Fe+CO_2\) \(\Rightarrow n_{CO}=n_{CO_2}=0,01mol\)
bạn xem lại đề bài nhé ý b không giải đc đâu

1./ Dẫn luồng khí H2 qua ống đựng CuO:
CuO + H2 → Cu + H2O
a a a
Khối lượng chất rắn giảm:
Δm = m(CuO pư) - m(Cu) = 80a - 64a = 80 - 72,32 = 7,68g
⇒ a = 7,68/16 = 0,48g
Số mol H2 tham gia pư: n(H2) = 0,48/80% = 0,6mol
Theo ĐL bảo toàn nguyên tố, số mol HCl tham gia pư là: n(HCl pư) = 2.n(H2) = 1,2mol
Theo ĐL bảo toàn khối lượng:
m(hh rắn) + m(HCl pư) = m(muối) + m(H2) ⇒ m(muối) = m(hh rắn) + m(HCl pư) - m(H2)
⇒ m(muối) = 65,45 + 0,12.36,5 - 0,6.2 = 108,05g
Gọi x, y là số mol Al và Zn có trong hh KL ban đầu.
m(hh KL) = m(Al) + m(Zn) = 27x + 65y = 40,6g
m(muối) = m(AlCl3) + m(ZnCl2) = 133,5x + 136y = 108,05g
⇒ x = 0,3mol và y = 0,5mol
Khối lượng mỗi kim loại:
m(Al) = 0,3.27 = 8,1g; m(Zn) = 65.0,5 = 32,5g
Thành phần % khối lượng mỗi kim loại:
%Al = 8,1/40,6 .100% = 19,95%
%Zn = 32,5/40,6 .100% = 80,05%

Đáp án B
Đặt n C O P T 1 = x m o l ; n C O 2 P T 2 = y m o l
C + H 2 O → t 0 C O + H 2 ( 1 ) x x m o l C + 2 H 2 O → t 0 C O 2 + 2 H 2 ( 2 ) y 2 y m o l C O + C u O → t 0 C u + C O 2 ( 3 ) x x m o l H 2 + C u O → t 0 C u + H 2 O ( 4 ) ( x + 2 y ) ( x + 2 y ) m o l
Hỗn hợp khí X có x mol CO, y mol CO2; (x+2y) mol H2
→ x + y + x+ 2y= 15,68/22,4= 0,7 mol hay 2x +3y= 0,7 mol (I)
Tổng số mol Cu là x+x+2y= 2x+ 2y mol
3Cu + 8HNO3 → 3Cu(NO3)2+ 2NO+ 4H2O (1)
Theo PT (1): nNO= 2/3. nCu= 2/3 (2x+2y)= 0,4 (II)
Giải hệ (I, II) ta có: x= 0,2; y= 0,1
% V C O = % n C O = 0 , 2 0 , 7 . 100 % = 28 , 57 %

a) \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,2---------------------->0,3
=> VH2 = 0,3.22,4 = 6,72 (l)
b)
\(n_{CuO}=\dfrac{32}{80}=0,4\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ: \(\dfrac{0,4}{1}>\dfrac{0,3}{1}\) => CuO dư, H2 hết
PTHH: CuO + H2 --to--> Cu + H2O
0,3<--0,3------->0,3
=> Rắn sau pư gồm \(\left\{{}\begin{matrix}Cu:0,3\left(mol\right)\\CuO\left(dư\right):0,1\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,3.64}{0,3.64+0,1.80}.100\%=70,59\%\\\%m_{CuO}=\dfrac{0,1.80}{0,3.64+0,1.80}.100\%=29,41\%\end{matrix}\right.\)

nZn = 13/65 = 0,2 (mol)
PTHH: Zn + H2SO4 -> ZnSO4 + H2
Mol: 0,2 ---> 0,2 ---> 0,2 ---> 0,2
VH2 = 0,2 . 22,4 = 4,48 (l)
nCuO = 32/80 = 0,4 (mol)
PTHH: CuO + H2 -> (r°) Cu + H2O
LTL: 0,4 > 0,2 => CuO dư
nCuO (p/ư) = nCu = 0,2 (mol)
mCuO (dư) = (0,4 - 0,2) . 80 = 16 (g)
mCu = 0,2 . 64 = 12,8 (g)
%mCuO = 16/(16 + 12,8) = 55,55%
%mCu = 100% - 55,55 = 45,45%
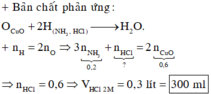

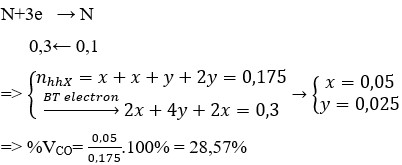
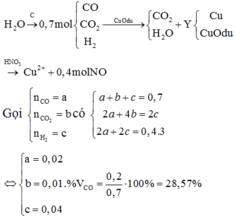
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{CuO}=\dfrac{32}{80}=0,4\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ: \(\dfrac{0,4}{1}>\dfrac{0,3}{1}\) => H2 hết, CuO dư
PTHH: CuO + H2 --to--> Cu + H2O
0,3<--0,3
CuO + H2SO4 --> CuSO4 + H2O
0,1--->0,1
=> \(V_{dd.H_2SO_4}=\dfrac{0,1}{1}=0,1\left(l\right)\)