trộn h2 và o2 theo tỉ lệ về khối lượng tương ứng là 3:8 ta được hỗn hợp khí Q.Cho nổ hỗn hợp khí Q trong bình kín đến phản ứng hoàn toàn rồi đưa về nhiệt độ ban đầu thì thấy thể tích còn lại là 1.792 lít .tính thể tích khí Q đã phản ứng ở đktc.Giải đầy đủ giúp em với ạ!Em cảm ơn !
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(\dfrac{mH2}{mO2}\)=\(\dfrac{3}{8}\)=x
=>;mH2=x=>nH2=\(\dfrac{3x}{2}\)mol
m02=\(\dfrac{8x}{32}\)=\(\dfrac{x}{4}\)mol
PTHH: 2H2 + O2 to→ 2H2O
xét: \(\dfrac{3x}{2}\);\(\dfrac{3x}{12}\)
h2 dư, o2 hết
nh2dư=\(\dfrac{3x}{2}-\dfrac{3x}{12}\)\(=\dfrac{15x}{12}\)=\(\dfrac{1,792}{22,4}\)=0,08(mol)
=>x=\(\dfrac{0,08.12}{15}\)=0,064
nO2=\(\dfrac{0,064}{4}\)=0,016(mol)
nH2=\(\dfrac{0,064.3}{2}\)=0,096(mol)
VQ(đktc)=22,4(0,016+0,096)=2,5088(lít)

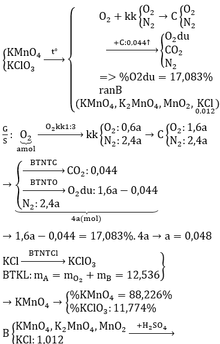
Đáp án B
Từ mKCl = 0,894g => mY = 10,994g
Đặt nO2 tạo ra = x => nkk = 3x có nO2 = 0,75x và nN2 = 2,25x (mol)
, nCO2 = nC = 0,044 mol => nO2 dư = (x + 0,75x) – 0,044 (mol)
=> nT = nCO2.100/22,92 = nO2 dư + nN2 + nCO2
=> 1,75x – 0,044 + 2,25x + 0,044 = 0,192
=> x = 0,048 mol
=> m = mY + mO2 tạo ra = 12,53g
=>B

a, Áp suất trong bình không thay đổi vì quá trình đốt cháy lưu huỳnh trong hỗn hợp X là quá trình xảy ra ở áp suất không đổi và sau khi đốt cháy, các sản phẩm khí sinh ra có cùng nhiệt độ và áp suất với hỗn hợp ban đầu.
b,Để tính phần trăm thể tích của hỗn hợp khí Y, ta cần biết tỉ lệ mol của các khí trong hỗn hợp Y. Theo phương trình phản ứng, khi đốt cháy lưu huỳnh trong hỗn hợp X, ta có:
S + O2 → SO2
Vì tỉ lệ mol giữa N2, O2 và SO2 trong hỗn hợp X là 2:1:1 nên khi đốt cháy hết lưu huỳnh, tỉ lệ mol giữa N2 và O2 trong hỗn hợp Y sẽ là 2:5. Do đó, ta có:
Tổng số mol khí trong hỗn hợp Y: 2 + 5 = 7 (vì tỉ lệ mol giữa N2 và O2 là 2:5)
Phần trăm thể tích của hỗn hợp Y: \(d\dfrac{Y}{X}\) = \(\dfrac{V_Y}{V_X}\) = \(\dfrac{n_Y.\dfrac{RT}{P}}{n_X.\dfrac{RT}{P}}=\dfrac{n_Y}{n_X}\) = 7/4 ≈ 175%
Vậy phần trăm thể tích của hỗn hợp khí Y là khoảng 175%.
c, Ta có:
\(d\dfrac{Y}{X}=\dfrac{V_Y}{V_X}=\dfrac{n_Y.\dfrac{RT}{P}}{n_X.\dfrac{RT}{P}}=\dfrac{n_Y}{n_X}\)
Với mỗi mol lưu huỳnh đốt cháy, số mol khí trong hỗn hợp Y tăng thêm 2, do đó nY = nX + 2 nhân số mol lưu huỳnh đốt cháy.
Từ đó suy ra: dY/X = (nX + 2 . số mol lưu huỳnh đốt cháy) / nX = 1 + 2 . số mol lưu huỳnh đốt cháy / nX
Do đó:
1 dY/X 1,21 tương đương với (dY/X) / 1,1684 = 1 + 2 . số mol lưu huỳnh đốt cháy / nX / 1,1684
=> 1,21 / 1,1684 - 1 = 2 . số mol lưu huỳnh đốt cháy / nX
=> số mol lưu huỳnh đốt cháy / nX = 0,0217
=> số mol lưu huỳnh đốt cháy = 0,0217 . nX
Vậy khi lượng lưu huỳnh biến đổi, 1 dY/X tăng thêm 2 . 0,0217 = 0,0434.

Có sự thay đổi số mol hỗn hợp khí xảy ra trong các phản ứng đốt cháy, hoặc đôi khi không thay đổi.
C/S + O2 → CO2/ SO2 (1)
2Al +3/2O2 → Al2O3 (2)
C, S hay A1, chúng là các chất rắn được đem đốt cháy với oxi hoặc một hỗn hợp khí chứa oxi,… và sau phản ứng người ta thu được một khí/hỗn hợp khí mới,…
Trong nhiều trường hợp, ta cần so sánh số mol hỗn hợp khí mới và cũ, như trong tình huống (1), hai giá trị này bằng nhau, tình huống (2) thì khác, khi có oxit tạo thành, tổng số mol khí sẽ giảm.
Với bài tập này, phản ứng của cacbon với oxi xảy ra và số mol hỗn hợp khí không thay đổi, đó chỉ là một sự thay thế như tăng giảm khối lượng vậy, O2 trở thành CO2 theo tỉ lệ 1:1 → nZ = nT
Bảo toàn nguyên tố C: nC/T = nCO2/T = 0,528/12 =0,044
→nT = 0,044/22,92% = 0,192 = nZ → nO2 trộn = 0,192/4 =0,048
→m = mY + mO2 = 0,894/8,132% + 32.0,048 = 12,5296
Chọn đáp án C

Đáp án : D
Phần 1: Trong cùng điều kiện nhiệt độ áp suất thì tỉ lệ về thể tích chính là tỉ lệ về số mol
→ VH2 pư = Vtrước -Vsau = 0,25. ( 11,2 + 6,72) = 4,48 lít < 6,72 lít → H2 dư và anken phản ứng hết
Vậy H chứa anken : 4,48 lít và ankan : 11.2 - 4,48 = 6,72 lít
→ nX : nY = 6,72 : 4,48 = 3: 2
Phần 2: Gọi số mol của X Cn H2n+ 2 là 3x và Y Cm H2m là 2x mol
Có 3x.( 14n+ 2) + 2x . 14m = 80 và 3x.n + 2xm = 5,5
→ 14. ( 3x.n + 2xm ) + 6x = 80 → x = 0,5
Có C tb =
5
,
5
5
.
0
,
5
= 2,2 → loại A
Sử dụng đường chéo Ctb = 2,2 và tỉ lệ 3:2 thấy n= 1 và m = 4 thỏa mãn.
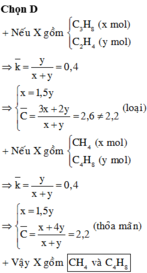
Gọi số mol H2, O2 là a, b (mol)
Ta có: \(\dfrac{m_{H_2}}{m_{O_2}}=\dfrac{3}{8}\)
=> \(\dfrac{2a}{32b}=\dfrac{3}{8}\Rightarrow\dfrac{a}{b}=\dfrac{6}{1}\) hay a = 6b
PTHH: 2H2 + O2 --to--> 2H2O
Xét tỉ lệ: \(\dfrac{6b}{2}>\dfrac{b}{1}\) => H2 dư, O2 hết
PTHH: 2H2 + O2 --to--> 2H2O
2b<---b
=> \(n_{H_2\left(dư\right)}=6b-2b=4b=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
=> b = 0,02 (mol)
=> a = 0,12 (mol)
=> VQ = (0,02 + 0,12).22,4 = 3,136 (l)