Một nguyên tử x có tổng số hạt là 58, số hạt trong nhân lớn hơn vỏ là 20 hạt a) tính nguyên tử khối b) cho biết mỗi lớp x có bao nhiêu electron
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(X(2p, n)\Leftrightarrow \begin{cases} 2p+n=58\\ p+n=20+e \end{cases}\Leftrightarrow \begin{cases} 2p+n=58\\ p+n=20+p \end{cases}\Leftrightarrow \begin{cases} p=e=20\\ n=19\end{cases} \to Kali\)

a: Theo đề, ta có hệ phương trình:
2Z+N=58 và Z+N-Z=20
=>N=20 và Z=19
b: Số Z là 19
=>Nguyên tử đó là K
Nguyên tử khối là M=39

`#3107.101107`
a.
Gọi số hạt proton, neutron, electron trong nguyên tử X lần lượt là `p, n, e`
Tổng số hạt trong nguyên tử X là `48`
`=> p + n + e = 48`
Mà trong nguyên tử, số `p = e`
`=> 2p + n = 48`
Mà số hạt `p = n`
`=> 3p = 48`
`=> p = 48 \div 3`
`=> p = 16`
Vậy, số `p = n = e = 16`
b.
Khối lượng nguyên tử X là: `16 + 16 = 32` (amu)
c.
Bạn tham khảo mô hình NT X:
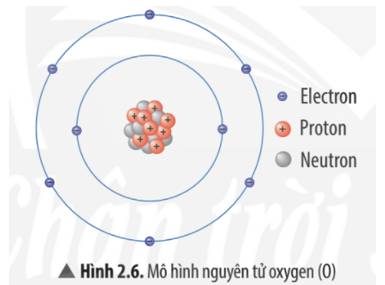
- X có `3` lớp electron
- X có `6` electron lớp ngoài cùng.

Ta có hệ phương trình:
\(\begin{cases}2Z+N=58\\P+N=20+E\end{cases}\) vì E=P=Z
<=>\(\begin{cases}2Z+N=58\\Z+N=20+Z\end{cases}\)
<=>\(\begin{cases}N=20\\Z=19\end{cases}\)
vì Z=19=>E=19 vậy ta có cấu hình electron như sau:
*1S22S22P63S23P64S1
\(n=\frac{11,7}{39,1}=0,3\) mol
2K+2H2O => 2KOH +H2
2 1
0,3 =>0,15 mol
=>Vh2= 0,15 . 22,4= 3,36 (lít)
Không có gì có bài nào cứ nhờ mình, giúp
được thì mình sẽ giúp OK.

Để giải bài toán này, chúng ta sẽ thực hiện các bước sau:
### Phần a: Tính số hạt mỗi loại của nguyên tử X
Gọi số proton, neutron và electron của nguyên tử X lần lượt là \( p, n, e \).
1. Tổng số hạt proton, neutron và electron là 52:
\[ p + n + e = 52 \]
2. Số hạt mang điện nhiều hơn số hạt không mang điện là 16:
\[ p + e - n = 16 \]
Vì nguyên tử trung hòa về điện tích, số proton bằng số electron:
\[ p = e \]
Do đó, chúng ta có thể thay \( e \) bằng \( p \) trong các phương trình trên:
\[ p + n + p = 52 \]
\[ 2p + n = 52 \quad \text{(1)} \]
\[ p + p - n = 16 \]
\[ 2p - n = 16 \quad \text{(2)} \]
Giải hệ phương trình (1) và (2):
Từ phương trình (1):
\[ n = 52 - 2p \]
Thay vào phương trình (2):
\[ 2p - (52 - 2p) = 16 \]
\[ 2p - 52 + 2p = 16 \]
\[ 4p - 52 = 16 \]
\[ 4p = 68 \]
\[ p = 17 \]
Vậy:
\[ p = 17 \]
\[ e = 17 \]
Thay vào phương trình (1) để tìm \( n \):
\[ 2p + n = 52 \]
\[ 2(17) + n = 52 \]
\[ 34 + n = 52 \]
\[ n = 18 \]
Vậy số hạt của nguyên tử X là:
- Proton: \( p = 17 \)
- Neutron: \( n = 18 \)
- Electron: \( e = 17 \)
### Phần b: Số electron trong mỗi lớp của nguyên tử X
Với số proton \( p = 17 \), nguyên tố X là Clo (Cl). Cấu hình electron của Cl là:
\[ 1s^2 2s^2 2p^6 3s^2 3p^5 \]
Do đó, số electron trong mỗi lớp là:
- Lớp 1: 2 electron
- Lớp 2: 8 electron
- Lớp 3: 7 electron
### Phần c: Tính nguyên tử khối của X
Nguyên tử khối của X là tổng khối lượng của các proton và neutron, vì khối lượng của electron rất nhỏ so với proton và neutron.
Khối lượng của X:
\[ \text{Nguyên tử khối} = p \cdot m_p + n \cdot m_n \]
\[ \text{Nguyên tử khối} = 17 \cdot 1.013 + 18 \cdot 1.013 \]
\[ \text{Nguyên tử khối} = 35 \cdot 1.013 \]
\[ \text{Nguyên tử khối} \approx 35.455 \]
### Phần d: Tính khối lượng bằng gam của X
Biết khối lượng của 1 đơn vị khối lượng nguyên tử (amu) là:
\[ 1 \, \text{amu} = \frac{1.9926 \times 10^{-23} \, \text{gam}}{12} \]
\[ 1 \, \text{amu} = 1.6605 \times 10^{-24} \, \text{gam} \]
Khối lượng của nguyên tử X bằng gam:
\[ \text{Khối lượng} \approx 35.455 \, \text{amu} \]
\[ \text{Khối lượng} \approx 35.455 \times 1.6605 \times 10^{-24} \, \text{gam} \]
\[ \text{Khối lượng} \approx 5.89 \times 10^{-23} \, \text{gam} \]
Vậy, khối lượng của nguyên tử X xấp xỉ \( 5.89 \times 10^{-23} \, \text{gam} \).

a, Số electron: (54 - 20) : 2 = 17 (hạt)
Tổng số proton và neutron: 54 - 17 = 37 (hạt)
Ta có: số e = số p = 17
=> số n = 37 - 17 = 20
Gọi số electron là Z, số notron là N
Ta có 2Z + N =58
Z+N-Z=20
--> N=20 Z=19
a) A=Z+N=20+19=38
b)1s2 2s2 2p6 3s2 3p6 4s1