cho 80g Fe2O3 tác dụng với 67,2 l khí H2 (đktc)
a/sau phản ứng chất còn dư và dư bao nhiêu gam
b/ Tính mFE tạo thành
cảm ơn mn
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a.Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right);n_{HCl}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\\ LTL:\dfrac{0,2}{1}< \dfrac{0,5}{2}\Rightarrow HCldư\\ n_{HCl\left(pứ\right)}=2n_{Zn}=0,4\left(mol\right)\\\Rightarrow m_{HCl\left(dư\right)}=\left(0,5-0,4\right).36,5=3,65\left(g\right)\\ b.n_{ZnCl_2}=n_{Zn}=0,2\left(mol\right)\\ \Rightarrow m_{ZnCl_2}=0,2.136=27,2\left(g\right)\\ c.n_{H_2}=n_{Zn}=0,2\left(mol\right)\\ \Rightarrow V_{H_2}=0,2.22,4,=4,48\left(l\right)\\ d.3H_2+Fe_2O_3-^{t^o}\rightarrow2Fe+3H_2O \\ n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12\left(mol\right)\\ LTL:\dfrac{0,2}{3}< \dfrac{0,12}{1}\Rightarrow Fe_2O_3dưsauphảnứng\\ \Rightarrow n_{Fe}=\dfrac{2}{3}n_{H_2}=\dfrac{2}{15}\left(mol\right)\\ \Rightarrow m_{Fe}=\dfrac{2}{15}.56=7,467\left(g\right)\)
a) n\(Zn\)=\(\dfrac{m}{M}\)=\(\dfrac{13}{65}\)=0,2(mol)
n\(HCl\)=\(\dfrac{m}{M}\)=\(\dfrac{18,25}{36,5}=\)0,5(mol)
PTHH : Zn + 2HCl->ZnCl\(2\) + H\(2\)
0,2 0,5
Lập tỉ lệ mol : \(^{\dfrac{0,2}{1}}\)<\(\dfrac{0,5}{2}\)
n\(Zn\) hết , n\(HCl\) dư
-->Tính theo số mol hết
Zn + 2HCl->ZnCl\(2\) + H\(2\)
0,2 -> 0,4 0,2 0,2
n\(HCl\) dư= n\(HCl\)(đề) - n\(HCl\)(pt)= 0,5 - 0,4 = 0,1(mol)
m\(HCl\) dư= 0,1.36,5 = 3,65(g)
b) m\(ZnCl2\) = n.M= 0,2.136= 27,2 (g)
c)V\(H2\)=n.22,4=0,2.22,4=4,48(l)
d) n\(Fe\)\(2\)O\(3\)=\(\dfrac{m}{M}\)=\(\dfrac{19,2}{160}\)=0,12 (mol)
3H2 +Fe2O3 → 2Fe + 3H2O
0,2 0,12
Lập tỉ lệ mol: \(\dfrac{0,2}{3}\)<\(\dfrac{0,12}{1}\)
nH2 hết .Tính theo số mol hết
\(HCl\)
3H2 +Fe2O3 → 2Fe + 3H2O
0,2-> 0,2
m\(Fe\)=n.M= 0,2.56= 11,2(g)

a) $Fe + H_2SO_4 \to FeSO_4 + H_2$
b) Ta thấy :
$n_{Fe} = \dfrac{5,6}{56} = 0,1 > n_{H_2SO_4} = \dfrac{1,96}{98} = 0,02$
Do đó Fe dư
$n_{Fe\ pư} = n_{H_2SO_4} = 0,02(mol)$
$m_{Fe\ dư} = 5,6 - 0,02.56 = 4,48(gam)$
c)
$n_{FeSO_4} = n_{H_2SO_4} = 0,02(mol) \Rightarrow m_{FeSO_4} = 0,02.152 = 3,04(gam)$
d)
$n_{H_2} = n_{H_2SO_4} = 0,02(mol)$
$V_{H_2} = 0,02.22,4 = 0,448(lít)$
nFe=5,6/56=0,1(mol)
nH2SO4=1,96/98=0,02(mol)
a) PTHH: Fe + H2SO4 -> FeSO4 + H2
b) Ta có: 0,02/1 < 0,1/1
=> Fe dư, H2SO4 hết => Tính theo nH2SO4.
=> nFe(p.ứ)=nFeSO4=nH2=nH2SO4=0,02(mol)
=>nFe(dư)=0,1 - 0,02=0,08(mol)
c) =>mFe(dư)= 0,08.56=4,48(g)
d) V(H2,đktc)=0,02.22,4=0,448(l)
Chúc em học tốt!

\(a,n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\\ n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
b, LTL: \(\dfrac{0,4}{4}>\dfrac{0,6}{3}\) => O2 dư
Theo pthh: \(\left\{{}\begin{matrix}n_{O_2\left(pư\right)}=\dfrac{3}{4}n_{Al}=\dfrac{3}{4}.0,4=0,3\left(mol\right)\\n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=\dfrac{1}{2}.0,4=0,2\left(mol\right)\end{matrix}\right.\)
=> VO2 (dư) = (0,6 - 0,3).22,4 = 6,72 (l)
c, mAl2O3 = 0,2.102 = 20,4 (g)
\(n_{Al}=\dfrac{10,8}{27}=0,4mol\)
\(n_{O_2}=\dfrac{13,44}{22,4}=0,6mol\)
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
Xét: \(\dfrac{0,4}{4}\) < \(\dfrac{0,6}{3}\) ( mol )
0,4 0,3 0,2 ( mol )
Chất dư là O2
\(m_{O_2\left(dư\right)}=\left(0,6-0,3\right).32=9,6g\)
\(m_{Al_2O_3}=0,2.102=20,4g\)

Số mol của kẽm
nZn = \(\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
Số mol của axit clohidric
nHCl = \(\dfrac{m_{HCl}}{M_{HCl}}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
Pt : Zn + 2HCl → ZnCl2 + H2\(|\)
1 2 1 1
0,3 0,4 0,2 0,2
a) Lập tỉ số só sánh : \(\dfrac{0,3}{1}>\dfrac{0,4}{2}\)
⇒ Zn dư , HCl phản ứng hết
⇒ Tính toán dựa vào số mol của HCl
Số mol dư của kẽm
ndư = nban đầu - nmol
= 0,3 - (\(\dfrac{0,4.1}{2}\))
= 0,1 (mol)
Khối lượng dư của kẽm
mdư = ndư . MZn
= 0,1 . 65
= 6,5 (g)
b) Số mol của khí hidro
nH2 = \(\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
Thể tích của khí hidro ở dktc
VH2 = nH2 . 22,4
= 0,2 . 22,4
= 4,48 (l)
Số mol của muối kẽm clorua
nZnCl2 = \(\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
Khối lượng của muối kẽm clorua
mznCl2 = nZnCl2 . MZnCl2
= 0,2. 136
= 27,2 (g)
c) 4H2 + Fe3O4 → (to) 3Fe + 4H2O\(|\)
4 1 3 4
0,2 0,15
Số mol của sắt
nFe = \(\dfrac{0,2.3}{4}=0,15\left(mol\right)\)
Khối lượng của sắt
mFe = nFe. MFe
= 0,15 . 56
= 8,4 (g)
Chúc bạn học tốt

a) \(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
\(n_{HCl}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
Xét tỉ lệ: \(\dfrac{0,1}{2}< \dfrac{0,4}{6}\) => Al hết, HCl dư
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,1--->0,3------>0,1---->0,15
=> mHCl = (0,4 - 0,3).36,5 = 3,65 (g)
b) VH2 = 0,15.22,4 = 3,36 (l)
\(n_{Al}=\dfrac{m_{Al}}{M_{Al}}=\dfrac{2,7}{27}=0,1mol\)
\(n_{HCl}=\dfrac{m_{HCl}}{M_{HCl}}=\dfrac{14,6}{36,5}=0,4mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,1 < 0,4 ( mol )
0,1 0,3 0,15 ( mol )
a. Chất còn dư là HCl
\(m_{HCl}=n_{HCl}.M_{HCl}=\left(0,4-0,3\right).36,5=3,65g\)
\(V_{H_2}=n_{H_2}.22,4=0,15.22,4=3,36l\)

nFe = 2.8/56 = 0.05 (mol)
nHCl = 14.6/36.5 = 0.4 (mol)
Fe + 2HCl => FeCl2 + H2
1.........2
0.05......0.4
LTL : 0.05/1 < 0.4/2
=> HCl dư
mHCl (dư) = ( 0.4 - 0.1 ) * 36.5 = 10.95 (g)
VH2 = 0.05*22.4 = 1.12 (l)
nHCl (dư) = 0.4 - 0.1 = 0.3 (mol)
mFe cần thêm = 0.3/2 * 56 = 8.4 (g)

\(a,PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ b,n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\ n_{HCl}=2\cdot0,15=0,3\left(mol\right)\)
Vì \(\dfrac{n_{Zn}}{1}>\dfrac{n_{HCl}}{2}\) nên sau p/ứ Zn dư
\(\Rightarrow n_{Zn}=\dfrac{1}{2}n_{HCl}=0,15\left(mol\right)\\ \Rightarrow m_{Zn}=0,15\cdot65=9,75\\ \Rightarrow m_{Zn\left(dư\right)}=13-9,75=3,25\left(g\right)\\ c,n_{H_2}=n_{Zn}=0,15\left(mol\right)\\ \Rightarrow V_{H_2}=0,15\cdot22,4=3,36\left(l\right)\)

\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right);n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\\ PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ Vì:\dfrac{0,4}{1}>\dfrac{0,25}{1}\Rightarrow Fe.dư\\ n_{H_2}=n_{Fe\left(p.ứ\right)}=n_{H_2SO_4}=0,25\left(mol\right)\\ a,V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\\ b,n_{Fe\left(dư\right)}=0,4-0,25=0,15\left(g\right)\\ m_{Fe\left(dư\right)}=0,14.56=8,4\left(g\right)\)
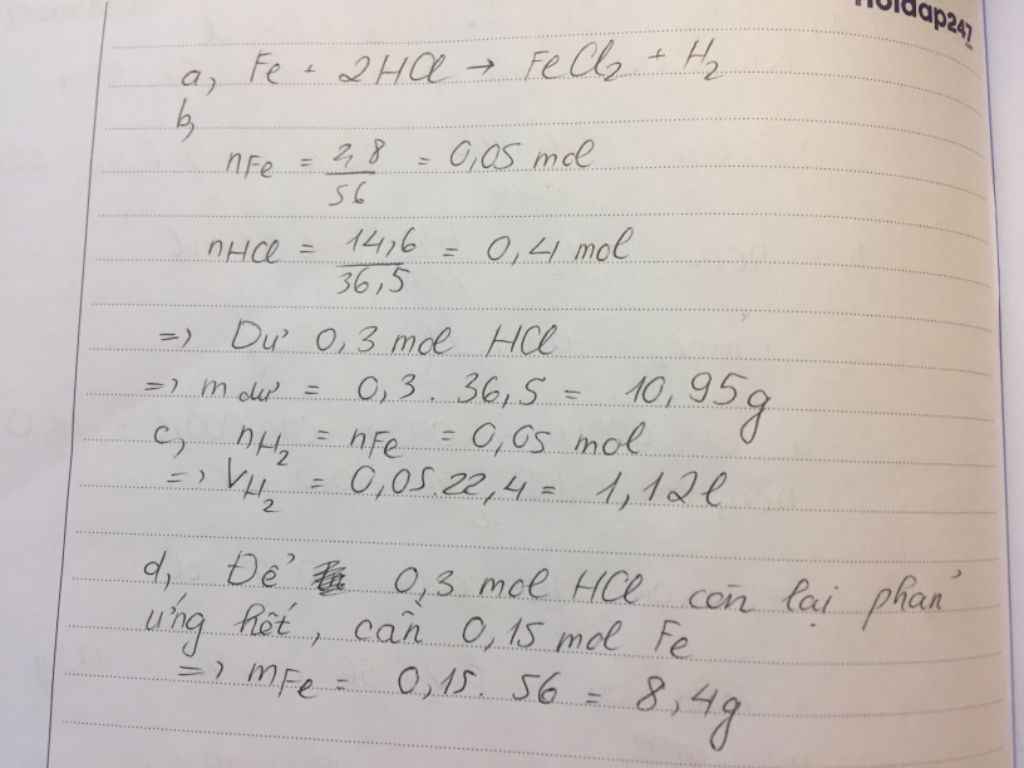

\(a,n_{Fe_2O_3}=\dfrac{80}{160}=0,5\left(mol\right)\\ n_{H_2}=\dfrac{67,2}{22,4}=3\left(mol\right)\)
PTHH: \(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
Trước: 0,5 3
Trong; 0,5 1,5 1
Sau: 0 1,5 1
Vì \(\dfrac{0,5}{1}< \dfrac{3}{3}\) nên H2 dư
\(m_{H_2\left(dư\right)}=1,5.2=3\left(g\right)\)
b, \(m_{Fe}=56.1=56\left(g\right)\)
nFe2O3 = 80 : 160 = 0,5 (mol)
nH2 = 67,2 : 22,4 =3 (mol)
pthh : Fe2O3 + 3H2 -t--> 4Fe + 3H2O
LTL
0,5/1 < 3/3 => H2 du
theo pt , nFe = 4nFe2O3 = 2 (mol)
=> mFe = 2 .56 = 112 (g)