Đốt cháy hoàn toàn 3,36 lít hỗn hợp metan và axetilencaanf dùng 15,68 lít khí oxi.Tính phần trăm thể tích mỗi khí ban đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{CH_4} = a\ mol ;n_{C_2H_6} = b\ mol\\ \Rightarrow a + b = \dfrac{3,36}{22,4}= 0,15(1)\\ CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ C_2H_6 + \dfrac{7}{2}O_2 \xrightarrow{t^o} 2CO_2 + 3H_2O\\ n_{CO_2} = a + 2b = \dfrac{4,48}{22,4} = 0,2(2)\\ (1)(2) \Rightarrow a = 0,1 ;b = 0,05\\ \Rightarrow \%V_{CH_4} = \dfrac{0,1}{0,15}.100\% = 66,67\%\\ \%V_{C_2H_6} = 100\% - 66,67\% = 33,33\%\)
\(n_{CH_4}=a\left(mol\right),n_{C_2H_6}=b\left(mol\right)\)
\(\Rightarrow a+b=0.15\left(mol\right)\left(1\right)\)
\(n_{CO_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(\Rightarrow a+2b=0.2\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.05\)
\(\%CH_4=\dfrac{0.1}{0.15}\cdot100\%=66.67\%\)
\(\%C_2H_6=33.33\%\)

CH4 -> CO2
C2H6 -> 2 CO2
Gọi nCH4 = x mol, nC2H6 = y mol
x + y = 0,15 (1)
x + 2y = 0,2 (2)
Nên: x = 0,1 mol, y = 0,05 mol
Vậy: % VCH4 = 66,67 % => %VC2H6 = 33,33 %

\(n_{hh}=\dfrac{3,36}{22,4}=0,15mol\)
\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{C_2H_2}=y\left(mol\right)\end{matrix}\right.\)
\(CH_4+2O_2\rightarrow CO_2+2H_2O\)
\(C_2H_2+\dfrac{5}{2}O_2\rightarrow2CO_2+H_2O\)
Từ hai pt trên:\(\Rightarrow\left\{{}\begin{matrix}x+y=0,15\\x+2y=0,2\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
\(\%V_{CH_4}=\dfrac{0,1}{0,1+0,05}\cdot100\%=66,67\%\)
\(\%V_{C_2H_2}=100\%-66,67\%=33,33\%\)
\(n_{CO_2}=\dfrac{V_{CO_2}}{22,4}=\dfrac{4,48}{22,4}=0,2mol\)
Gọi \(n_{CH_4}\) là x \(\Rightarrow V_{CH_4}=22,4x\)
\(n_{C_2H_2}\) là y \(\Rightarrow V_{C_2H_2}=22,4y\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
x x ( mol )
\(2C_2H_2+5O_2\rightarrow\left(t^o\right)4CO_2+2H_2O\)
y 2y ( mol )
Ta có:
\(\left\{{}\begin{matrix}22,4x+22,4y=3,36\\x+2y=0,2\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
\(\Rightarrow V_{CH_4}=22,4.0,1=2,24l\)
\(\Rightarrow V_{C_2H_2}=22,4.0,05=1,12l\)
\(\%V_{CH_4}=\dfrac{2,24}{3,36}.100=66,67\%\)
\(\%V_{C_2H_2}=100\%-66,67\%=33,33\%\)

a, \(CH_4+2O_2\underrightarrow{^{t^o}}CO_2+2H_2O\)
\(C_2H_4+3O_2\underrightarrow{^{t^o}}2CO_2+2H_2O\)
b, Gọi: \(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{C_2H_4}=y\left(mol\right)\end{matrix}\right.\) \(\Rightarrow x+y=\dfrac{4,48}{22,4}=0,2\left(mol\right)\left(1\right)\)
Theo PT: \(n_{O_2}=2n_{CH_4}+3n_{C_2H_4}=2x+3y=\dfrac{15,68}{22,4}=0,7\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=-0,1\\y=0,3\end{matrix}\right.\)
Đến đây thì ra số mol âm, bạn xem lại đề nhé.

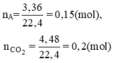
Gọi số mol của metan và etan lần lượt là x và y (mol)
Phương trình phản ứng:
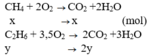
Vậy thành phần phần trăm về thể tích các khí trong hỗn hợp A là:
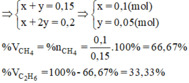

a) Gọi \(\left\{{}\begin{matrix}n_{C_2H_4}=a\left(mol\right)\\n_{C_3H_6}=b\left(mol\right)\end{matrix}\right.\left(a,b>0\right)\Rightarrow a+b=\dfrac{6,72}{22,4}=0,3\left(1\right)\)
PTHH:
\(C_2H_4+3O_2\xrightarrow[]{t^o}2CO_2+2H_2O\)
a-------->3a------>2a
\(2C_3H_6+9O_2\xrightarrow[]{t^o}6CO_2+6H_2O\)
b-------->4,5b---->3b
\(\Rightarrow n_{O_2}=3a+4,5b=\dfrac{23,52}{22,4}=1,05\left(2\right)\)
Từ \(\left(1\right),\left(2\right)\Rightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,2}{0,3}.100\%=66,67\%\\\%V_{C_3H_6}=100\%-66,67\%=33,33\%\end{matrix}\right.\)
b) \(V_{CO_2}=\left(0,2.2+0,1.3\right).22,4=15,68\left(l\right)\)

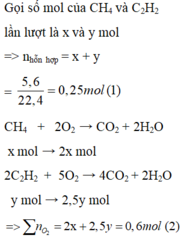

\(V_{CH_4} = a(lít) ; V_{C_2H_2} = b(lít) \Rightarrow a + b = 3,36(1)\\ CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ 2C_2H_2 + 5O_2 \xrightarrow{t^o} 4CO_2 + 2H_2O\\ V_{O_2} = 2a + \dfrac{5}{2}b = 15,68(2)\\ (1)(2) \Rightarrow a = -14,56<0\)
(Sai đề)