Câu 2.
Nhiệt phân hoàn toàn 31,6 gam KMnO4 sau phản ứng thấy thoát ra V (lít) khí oxi (đktc).
a) Viết PTHH của phản ứng trên và tính giá trị của V?
b) Để đốt cháy hoàn toàn 2,16 gam kim loại R (có hóa trị không đổi) cần dùng 60% lượng oxi sinh ra từ phản ứng trên. Hãy xác định kim loại R.

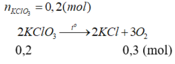

a.\(n_{KMnO_4}=\dfrac{m}{M}=\dfrac{31,6}{158}=0,2mol\)
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,2 0,1 ( mol )
\(V_{O_2}=n.22,4=0,1.22,4=2,24l\)
b.\(n_{O_2}=0,1.60\%=0,06mol\)
\(2R+\dfrac{1}{2}nO_2\rightarrow\left(t^o\right)R_2O_n\)
\(\dfrac{2,16}{M_R}\) \(\dfrac{2,16n}{M_R}\) ( mol )
\(\Rightarrow\dfrac{2,16n}{M_R}=0,06\)
\(\Rightarrow0,06M_R=2,16n\)
\(\Rightarrow M_R=36n\)
Biện luận:
-n=1 => Loại
-n=2 => Loại
-n=3 => \(M_R=108\) ( g/mol ) R là Bạc ( Ag )
Vậy R là Bạc (Ag)
Đề sai rồi, Ag không bị oxi hoá nha:v