Cho 500ml dung dịch NaOH aM vào 500ml dung dịch H2SO4 0,6M thu được dung dịch A. Lấy dung dịch A hoà tan hoàn toàn 0,53g Al2O3. a là:
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Bài tập vận dụng
VD1: Hoà tan hoàn toàn 7,45 gam KCI vào 200ml H2O thu đưoc dung dịch A. Tính nồng độ %, nồng độ mol/l
của dung dịch A.
VD2: Hoà tan hoàn toàn 0,2 mol NaOH vào 500ml H20 thu được dung dịch B. Tính nồng độ %, nồng độ mol/l
của dung dịch B.
VD3: Hoà tan hoàn toàn 2,8 gam KOH và 5,85 gam NaCl vào 600 ml H2O thu được dung dịch C. Tinh nồng độ
%, nồng độ mol/l của dung dịch C.
VD4: Hoà tan hoàn toàn 4,6 gam Na vào 100 gam H20 thu được dung dịch D. Tính nồng độ %, nồng độ mol/I
của dung dịch D.
VD5: Hoà tan hoàn toàn 2,74 gam Ba vào 200 gam H2O thu được dung dịch E. Tính nồng độ %, nồng độ mol/l
của dung dịch E.
VD6: Hoà tan hoàn toàn 5,85 gam K và 13,7 gam Ba vào 400ml H2O thu đưoc dung dịch F. Tính nồng đo %,
nồng đo mol/l của dung dịch F.
VD1:
\(n_{KCl}=\dfrac{7,45}{74,5}=0,1\left(mol\right)\\ V_{ddKCl}=V_{H_2O}=200\left(ml\right)=0,2\left(l\right)\\ C_{MddKCl}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)

a) PTHH: \(K_2O+H_2O\rightarrow2KOH\)
Ta có: \(n_{K_2O}=\dfrac{9,4}{94}=0,1\left(mol\right)\)
\(\Rightarrow n_{KOH}=0,2\left(mol\right)\) \(\Rightarrow C_{M_{KOH}}=\dfrac{0,2}{0,5}=0,4\left(M\right)\)
b) PTHH: \(2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\)
Theo PTHH: \(n_{H_2SO_4}=\dfrac{1}{2}n_{KOH}=0,1\left(mol\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{0,1\cdot98}{9,8\%}=100\left(g\right)\)
a) \(K_2O+H_2O\rightarrow2KOH\)
\(n_{KOH}=2n_{K_2O}=2.\dfrac{9,4}{94}=0,2\left(mol\right)\)
=> \(CM_{KOH}=\dfrac{0,2}{0,5}=0,4M\)
b) \(2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\)
0,2...........0,1
=> \(m_{ddH_2SO_4}=\dfrac{0,1.98}{9,8\%}=100\left(g\right)\)

Đáp án B
Ta có: nNaOH = 0,15 mol; nBa(OH)2 = 0,05 mol
Dung dịch Y chứa 0,15 mol Na+, 0,05 mol Ba2+, u mol AlO2- và v mol OH- dư
Định luật bảo toàn điện tích ta có u + v = 0,15 + 0,05.2 = 0,25 (1)
Ta có: nHCl = 0,32 mol và nH2SO4 = 0,04 mol→ nH+ = 0,4 mol; nSO4(2-) = 0,04 mol
→ nBaSO4 = 0,04 mol
Ta có: mkết tủa = 21,02 gam → nAl(OH)3 = 0,15 mol
Nếu Al(OH)3 chưa bị hòa tan thì nH+ = 0,4 = v + 0,15 (2)
Nếu Al(OH)3 đã bị hòa tan thì nH+ = 0,4 = v + 4u - 3.0,15 (3)
Giải hệ (1) và (2) ra vô nghiệm
Giải hệ (1) và (3) ra u = 0,2 và v = 0,05
Vậy Y gồm Na+ 0,15 mol; 0,05 mol Ba2+; 0,2 mol AlO2- và OH- dư (0,05 mol)
V lít dung dịch Z gồm 0,64V mol HCl và 0,08V mol H2SO4
→ nH+ = 0,8V mol và nSO4(2-) = 0,08 V mol
Khi Al(OH)3 max thì 0,8V = u+ v suy ra V = 0,3125
Suy ra nBaSO4 = 0,025 mol → mkết tủa = 21,425 gam
Khi BaSO4 max thì 0,08V = 0,05 suy ra V = 0,625
Suy ra nH+ = 0,8V = v + 4u-3.nAl(OH)3 → nAl(OH)3 = 7/60 mol → mkết tủa = 20,75 gam
Vậy mkết tủa max = 21,425 gam

nH2SO4 = nBaSO4 = 0,1
-> y = 0,2 (mol/l)
nAl2O3 = 0,01
TH1: Axit dư:
H2SO4 + 2NaOH —> Na2SO4 + 2H2O
0,25x 0,5x
3H2SO4 + Al2O3 —> Al2(SO4)3 + 3H2O
0,03 0,01
-> nH2SO4 = 0,25x + 0,03 = 0,1
-> x = 0,28 (mol/l)
TH2: NaOH dư:
H2SO4 + 2NaOH —> Na2SO4 + 2H2O
0,1 0,2
Al2O3 + 2NaOH —> 2NaAlO2 + H2O
0,01 0,02
-> nNaOH tổng = 0,5x = 0,22
-> x = 0,44 (mol/l)
Vậy \(\left[{}\begin{matrix}x=0,28\\x=0,44\end{matrix}\right.\)(mol/l)
y = 0,2 (mol/l)

Gọi số mol Na2O và Al2O3 lần lượt là x, y
Nhận thấy khi thêm 0,1 mol HCl vào dung dịch X thì thấy xuất hiện kết tủa
→ Trong dung dịch X chứa NaAlO2 a mol và NaOH :0,1 mol
Bảo toàn nguyên tố → nNa2O = (nNaOH + nNaAlO2):2 = (0,1 + a): 2
nAl2O3 = nNaAlO2 : 2 = a:2
Ta có phương trình : [(0,1 + a): 2 ]×62 + (a:2)×102 = 19,5→ → a= 0,2 mol
CMNaOH = 0,2M, CMNaAlO2 = 0,4M
Đáp án C

Số mol các chất là: ![]()
![]()
Đặt số mol các chất trong X là Al: a mol; Mg: b mol.
![]()
Sơ đồ phản ứng:
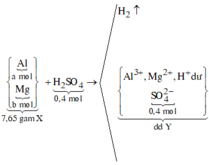
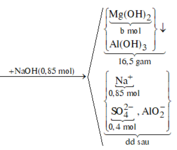
![]()
![]()
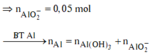
![]()
![]()
![]()
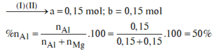
Đáp án A


nNaOH = 0,5a mol, nH2SO4 = 0,3 mol, nAl2O3 = 0,0052 mol
TH1: Dung dịch A chứa H2SO4 dư
2NaOH + H2SO4 ➝ Na2SO4 + 2H2O
0,5a 0,25a
➝ nH2SO4 dư = 0,3 - 0,25a (mol)
2Al + 3H2SO4 ➝ Al2(SO4)3 + 3H2
2(0,3-0,25a)/3 (0,3 - 0,25a)
➝ nAl = \(\dfrac{2\left(0,3-0,25a\right)}{3}=0,0052\) ➝ a = 1,1688
TH2: NaOH dư
2NaOH + H2SO4 ➝ Na2SO4 + 2H2O
0,6 0,3
➝ nNaOH dư = 0,5a - 0,6 mol
Al2O3 + 2NaOH ➝ 2NaAlO2 + H2O
(0,5a - 0,6)/2 (0,5a - 0,6)
➝ \(\dfrac{0,5a-0,6}{2}=0,0052\) ➝ a = 1,2208