1. Hòa tan hoàn toàn một lượng P2O5 vào 200 gam dung dịch H3PO4 10%. Sau đó phản ứng thu được dung dịch H3PO4 17,93%. Tính khối lượng P2O5 đã dùng?
2. Nung m gam thuốc tím chứa 10% tạp chất (không phản ứng) thu được 10,08 lít khí(đktc) thu được hỗn hợp chất rắn X.
a. Tính m biết H = 80%.
b. Tính khối lượng các chất trong hỗn hợp X.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
X gồm :
$PO_4^{3-} : a(mol)$
$HPO_4^{2-} : b(mol)$
$K^+ : 0,5(mol)$
Bảo toàn điện tích : $3a + 2b = 0,5$
Khối lượng rắn khan : $95a + 96b + 0,5.39 = \dfrac{193}{71}m$
Bảo toàn P : $142.0,5(a + b) = m$
Suy ra : a = 0,1 ; b = 0,1 ; m = 14,2
b)
$n_{BaHPO_4} = b = 0,1(mol)$
$n_{Ba_3(PO_4)_2} = 0,5a = 0,05(mol)$
$m_{Kết\ tủa} = 0,1.233 + 0,05.601 = 53,35(gam)$

Ta có: $n_{P_2O_5}=\frac{m}{141}(mol);n_{NaOH}=1,014(mol)$
$\Rightarrow n_{H_3PO_4}=\frac{m}{71}\Rightarrow n_{H_2O}=\frac{3m}{71}$
Bảo toàn khối lượng ta có:
\(\dfrac{98}{71}m+40,56=3m+\dfrac{3m}{71}.18\Rightarrow m=17,04\left(g\right)\)
\(n_{NaOH} = 0,507.2 = 1,014(mol)\)
Nếu rắn khan chứa :
\(\left\{{}\begin{matrix}Na^+:1,014\left(mol\right)\\PO_4^{3-}:x\left(mol\right)\\HPO_4^{2-}:y\left(mol\right)\end{matrix}\right.\)
Bảo toàn P : 0,5(x + y).142 = m
Muối : \(m_{muối}\) = 1,014.23 + 95x + 96y = 3m
Bảo toàn điện tích: 3x + 2y = 1,014
Suy ra: y =-0,432 <0 => Loại
\(\left\{{}\begin{matrix}Na^+:1,014\left(mol\right)\\PO_4^{3-}:a\left(mol\right)\\OH^-:b\left(mol\right)\end{matrix}\right.\)
Bảo toàn điện tích : 3a + b = 1,014
\(m_A\) = 1,014.23 + 95a + 17b = 3m
Bảo toàn P : 0,5a.142 = m
Suy ra: a = 0,24 ; b = 0,294; m = 17,04(gam)

1) Gọi số mol P2O5 là a (mol)
PTHH: P2O5 + 3H2O --> 2H3PO4
a----------------->2a
mH3PO4(tổng)=98.2a+10.200100=196a+20(g)��3��4(�ổ��)=98.2�+10.200100=196�+20(�)
mdd sau pư = 142a + 200 (g)
=> C%dd.sau.pư=196a+20142a+200.100%=18%�%��.���.�ư=196�+20142�+200.100%=18
=> a = 0.094 mol)
=> mP2O5 = 0,094.142 = 13.348(g)

a) 4P + 5O2 --to--> 2P2O5
b) \(n_P=\dfrac{24,8}{31}=0,8\left(mol\right)\)
PTHH: 4P + 5O2 --to--> 2P2O5
0,8--------------->0,4
=> mP2O5 = 0,4.142 = 56,8 (g)
c)
PTHH: P2O5 + 3H2O --> 2H3PO4
0,4--------------->0,8
=> mH3PO4 = 0,8.98 = 78,4 (g)

a, \(n_{P_2O_5}=\dfrac{21,3}{142}=0,15\left(mol\right)\)
PT: \(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
Theo PT: \(n_{H_3PO_4}=2n_{P_2O_5}=0,3\left(mol\right)\)
\(\Rightarrow m_{H_3PO_4}=0,3.98=29,4\left(g\right)\)
b, m dd sau pư = 21,3 + 300 = 321,3 (g)
\(\Rightarrow C\%_{H_3PO_4}=\dfrac{29,4}{321,3}.100\%\approx9,15\%\)

Đáp án A
nKOH = (400.10%)/(100%.56) = 5/7 (mol)
Gọi nP2O5 = x (mol) => nH3PO4 = 2x (mol)
KOH dư nên muối thu được là K3PO4 : 2x (mol)
Gọi nKOH dư là y (mol)
Ta có: 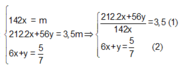
Thế (2) vào (1) => x = 0,09779 => mP2O5 = 142. 0,9779 = 13,88 (gam) ≈ 14(gam)


1) Gọi số mol P2O5 là a (mol)
PTHH: P2O5 + 3H2O --> 2H3PO4
a----------------->2a
\(m_{H_3PO_4\left(tổng\right)}=98.2a+\dfrac{10.200}{100}=196a+20\left(g\right)\)
mdd sau pư = 142a + 200 (g)
=> \(C\%_{dd.sau.pư}=\dfrac{196a+20}{142a+200}.100\%=17,93\%\)
=> a = 0,093 (mol)
=> mP2O5 = 0,093.142 = 13,206 (g)
2)
a) \(n_{O_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,9<-----------0,45<----0,45<----0,45
=> \(m_{KMnO_4\left(Pư\right)}=0,9.158=142,2\left(g\right)\)
=> \(m_{KMnO_4\left(tt\right)}=\dfrac{142,2.100}{80}=177,75\left(g\right)\)
=> \(m=\dfrac{177,75.100}{90}=197,5\left(g\right)\)
b)
X \(\left\{{}\begin{matrix}m_{K_2MnO_4}=0,45.197=88,65\left(g\right)\\m_{MnO_2}=0,45.87=39,15\left(g\right)\\m_{KMnO_4}=177,75-142,2=35,55\left(g\right)\\m_{tạp.chất}=197,5.10\%=19,75\left(g\right)\end{matrix}\right.\)