Cho 2,1 gam kim loại A hoá trị I vào nước dư thu được lượng H2 nhỏ hơn 1,12 lít khí ở(đkt). Nếu cho 8,2 gam kim loại A vào nước dư thì lượng H2 thoát ra vượt quá 2,24 lít ở (đkt). Xác định kim loại A ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Tham khảo:
2A+ 2H2O -> 2AOH+ H2
- TN1:
nH2= 0,05 mol
nA= 2,1/A mol
=> 1,05/A < 0,05
=> A > 21 (1)
- TN2:
nH2= 0,1 mol
nA= 8,2/A mol
=> 4,1/A > 0,1
=> A < 41 (2)
(1)(2) => 21 < A < 41
Vậy A= 23 (Na) hoặc A= 39 (K)

2A +H2O ----> H2 +A2O
trường hợp 1: nH2< 0,05 => nA< 0,1 => MA > 2,1/0,1=21
trường hợp 2:nH2>0,1 => nA> 0,2 => MA < 41
=> A là Rb(37,hóa trị I )
theo mik thì là như vậy :
2A +H2O ----> H2 +A2O
trường hợp 1: nH2< 0,05 => nA< 0,1 => MA > 2,1/0,1=21
trường hợp 2:nH2>0,1 => nA> 0,2 => MA < 41
=> A là Rb(37,hóa trị I )
Chúc bn học tốt

2A + H2O \(\rightarrow\) H2 + A2O
Trường hợp 1 : nH2 < 0,05 \(\Rightarrow\) nA < 0,1 \(\Rightarrow\) MA > 2,1/0,1 = 21
Trường hợp 2 : nH2 > 0,1 \(\Rightarrow\) nA > 0,2 \(\Rightarrow\) MA < 41
\(\Rightarrow\) A là Rb ( 37 , hóa trị 1 )

\(2A+2HCl\rightarrow2ACl+H_2\)
TH1:
\(n_A=\frac{2,1}{A}\left(mol\right)\)
\(\Rightarrow n_{H_2}=\frac{2,1}{2A}< \frac{1,12}{22,4}=0,05\)
\(\Leftrightarrow A>21\left(1\right)\)
TH2:
\(n_A=\frac{8,2}{A}\left(mol\right)\)
\(\Rightarrow n_{H_2}=\frac{8,2}{2A}>\frac{2,24}{22,4}=0,1\)
\(\Leftrightarrow A< 41\left(2\right)\)
Từ (1) và (2) ta suy ra A là Na hoặc K

\(n_{A\left(1\right)}=\frac{2,1}{A}\left(mol\right);n_{A\left(2\right)}=\frac{8,2}{A}\left(mol\right)\)
PTHH 1: 2A + 2H2O --> 2AOH + H2
\(\frac{2,1}{A}\) -------------------------> \(\frac{1,05}{A}\) (mol)
PTHH 2: 2A + 2H2O --> 2AOH + H2
\(\frac{8,2}{A}\) --------------------------> \(\frac{4,1}{A}\) (mol)
=> \(\frac{1,05}{A}< \frac{1,12}{22,4}\) ; \(\frac{4,1}{A}>\frac{2,24}{22,4}\)
=> \(\frac{1,05}{A}< 0,05\); \(\frac{4,1}{A}>0,1\)
=> 21<A<41 => A là Na,K
MIK NGHĨ ZẬY
\(2A+2H_2O\rightarrow2Aoh+H_2\)
- TN1:
\(n_{H2}=0,05\left(mol\right)\)
\(n_A=\frac{2,1}{A}\left(mol\right)\)
\(\Rightarrow\frac{1,05}{A}< 0,05\Rightarrow A>21\left(1\right)\)
- TN2:
\(n_{H2}=0,1\left(mol\right)\)
\(n_A=\frac{8,2}{A}\left(mol\right)\)
\(\Rightarrow\frac{4,1}{A}>0,1\Rightarrow A< 41\left(2\right)\)
\(\left(1\right)+\left(2\right)\Rightarrow21< A< 41\)
Vậy A= 23 (Na) hoặc A= 39 (K)

Chọn đáp án B
Ta có nZn = nH2 = 0,1 ⇒ mZn = 6,5 gam
⇒ mKim loại không tan = mCu = 8,2 – mZn = 1,7 gam

Nếu A không có K:
\(\%m_K=\dfrac{10,66}{29,34+10,66}\cdot100\%=26,65\%\ne29,35\%\\ R:Kali\\ K+H_2O->KOH+\dfrac{1}{2}H_2\\ M+2H_2O->M\left(OH\right)_2+H_2\\ n_K=a,n_M=b\left(mol\right)\\ n_{H_2}=0,5a+b=\dfrac{5,376}{22,4}=0,24mol\\ \%m_{K\left(B\right)}=\dfrac{39a+10,66}{29,34+10,66}\cdot100=29,35\\ a=0,028\\ b=0,226\\ M_M=\dfrac{29,34-39\cdot0,028}{0,226}=125\left(g\cdot mol^{^{-1}}\right)\)
Vậy không có kim loại kiềm thổ thoả đề
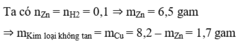
2A + H20 ---> H2 + A20
Trường hợp 1 : nH2 < 0,05 ⇒⇒ nA < 0,1 => MA > 2,1 / 0,1 = 21
Trường hợp 2 : nH2 > 0,1 => nA > 0,2 => MA < 41
=> A là Rb ( 37 , hóa trị l )