Nhiệt phân 98 gam KClO3 (có xúc tác MnO2), sau một thời gian thu được 93,2 gam chất rắn và khí A. Cho toàn bộ khí A phản ứng hết với hỗn hợp kim loại X gồm Mg, Fe thu được hỗn hợp chất rắn Y cân nặng 15,6 gam. Hoàn tan hoàn toàn hỗn hợp Y bằng dung dịch H2SO4 đặc nóng, dư thu được 0,56 lít khí SO2 (đktc, sản phẩm khử duy nhất của S+6). Tính thành phần % khối lượng của Mg trong hỗn hợp X.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
B T K L : m O 2 = m K M n O 4 - m c r a n = 3 , 84 g ⇒ n O 2 = 0 , 12 m o l ⇒ n O = 0 , 24 m o l m M g , F e = m o x i t - m O = 13 , 04 - 0 , 24 . 16 = 9 , 2 g a m M g : x m o l F e : y m o l
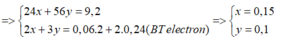
⇒ % m M g = 39 , 13 %

Đáp án D:
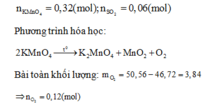
Gọi x và y lần lượt là số mol của Mg và Fe
=> 24x+56y = 9,2
Bảo toàn electron ta có
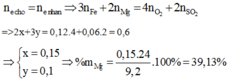

Đáp án : C
Bảo toàn khối lượng : mX = mO2 + mY
=> nO2 = 0,175 mol
Ta có : sản phẩm phản ứng với HCl chỉ có H2O là có Oxi
=> nO(Y) = nO(H2O) = 1/2nHCl = 0,4 mol
Bảo toàn O : nO(X) = 2nO2 + nO(Y) = 0,75 mol = 4nKMnO4 + 3nKClO3
Lại có : mX = 158nKMnO4 + 122,5nKClO3 = 30,225g
=> nKMnO4 = 0,075 ; nKClO3 = 0,15 mol
Nếu giả sử X + HCl => ne (X) = ne (O2) + ne(Y) + HCl
=> ne (Y) + HCl = 2nCl2 = 0,575 mol
=> x = 0,2875 mol

Đáp án B
Bảo toàn khối lượng: mO2 = 50,56 – 46,72 = 3,84(g) ⇒ nO2 = 0,12 mol.
● Đặt nMg = x; nFe = y. Bảo toàn electron: 2x + 3y = 0,12 × 4 + 0,06 × 2.
Bảo toàn khối lượng: mX = 13,04 – 0,12 × 32 = 24x + 56y ||⇒ giải hệ có:
x = 0,15 mol; y = 0,1 mol ⇒ %mMg = 39,13%

Đáp án B
Bảo toàn khối lượng:
mO2 = 50,56 – 46,72 = 3,84(g) ⇒ nO2 = 0,12 mol.
● Đặt nMg = x; nFe = y.
Bảo toàn electron: 2x + 3y = 0,12 × 4 + 0,06 × 2.
Bảo toàn khối lượng:
mX = 13,04 – 0,12 × 32 = 24x + 56y ||
⇒ giải hệ có:
x = 0,15 mol; y = 0,1 mol ⇒ %mMg = 39,13%
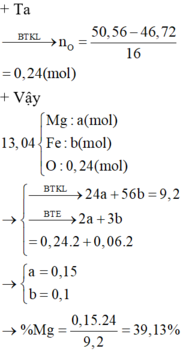


Áp dụng định luật bảo toàn khối lượng
mkhí A = mO2 = 98 - 93,2 = 4.8 (g)
⇔ nO2 = 0.15 (mol)
X + A ⇔ \(X\left\{{}\begin{matrix}Fe:a\\Mg:b\end{matrix}\right.\)(mol) + 0,15 mol O2 \(\underrightarrow{100\%}\) 15,6g chất rắn
⇔ mX = 56a + 24b = 15,6 - 0,15 . 32 = 10.8
15,6g Y \(\left\{{}\begin{matrix}Mg,Fe\\oxit\end{matrix}\right.\) ⇔ 15,6g \(\left\{{}\begin{matrix}Mg:a\\Fe:b\\O:0.3\end{matrix}\right.\) (mol)
Quá trình oxi hóa ________________ Quá trình khử
Mgo → Mg+2 + 2e O0 + 2e ⇒ O-2
a .................... 2a 0,3 ...... 0,6
Fe0 → Fe+3 + 3e S+6 + 2e → S+4
b ................... 3b 0.05 ← 0.025
Vậy 2a + 3b = 0,65
Giải ra a,b