người ta điều chế C2H2 từ than và đá vôi theo sơ đồ CaCO3 ----> CaO---->CaC2----> C2H2 với hiệu suất phản ứng trên sơ đồ. tính lượng đá vôi chứa 75% CaCO3 cần điều chế được 2,24 m3 C2H2 điều kiện tiêu chuẩn theo Sơ đồ trên
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PTHH: CaCO3 →to→CaO +CO2
+nCaO=nCO2=0,9(mol)
+mCaO=0,9.56=50,4(gam)
Hiệu suất pư là : \(\dfrac{50,4}{100}=0,504\)

\(m_{CaCO_3}=90\%\cdot1000=900\left(kg\right)\)
\(n_{CaCO_3}=\dfrac{900}{100}=9\left(kmol\right)\)
\(CaCO_3\underrightarrow{^{^{t^0}}}CaO+CO_2\)
\(9...............9\)
\(m_{CaO}=9\cdot56=504\left(kg\right)=0.504\left(tấn\right)\)
\(H\%=\dfrac{0.45}{0.504}\cdot100\%=89.28\%\)
1)
$2C + O_2 \xrightarrow{t^o} 2CO$
$m_{C\ pư} = 490 - 49 = 441(kg)$
$H = \dfrac{441}{490}.100\% = 90\%$
2)
$m_{CaCO_3} = 1000.90\% = 900(kg)$
$CaCO_3 \xrightarrow{t^o} CaO + CO_2$
$n_{CaCO_3\ pư} = n_{CaO} = \dfrac{0,45}{56} = 0,008(kmol)$
$H = \dfrac{0,008.100}{900}.100\% = 0,09\%$

Ta có: \(n_{C_2H_2}=\dfrac{168}{22,4}=7,5\left(mol\right)\)
PT: \(CaC_2+2H_2O\rightarrow Ca\left(OH\right)_2+C_2H_2\)
Theo PT: \(n_{CaC_2\left(LT\right)}=n_{C_2H_2}=7,5\left(mol\right)\)
Mà: H = 90%
\(\Rightarrow n_{CaC_2\left(TT\right)}=\dfrac{7,5}{90\%}=\dfrac{25}{3}\left(mol\right)\)
\(\Rightarrow m_{CaC_2\left(TT\right)}=\dfrac{25}{3}.64=\dfrac{1600}{3}\left(g\right)\)
Mà: Đất đèn chứa 80% CaC2.
⇒ m đất đèn = 1600/3 : 80% = 2000/3 (g)

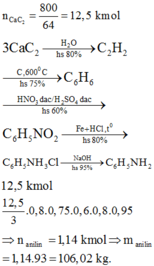
Chọn đáp án A
Chú ý : Giai đoạn cuối cùng có 1C bị biến mất nên cần chú ý khi BTNT.C
Cần nhớ khi (H=100%).
Vậy V=5.0,9.0,75.0,6.0,8.0,95.22,4=34,47(lit)
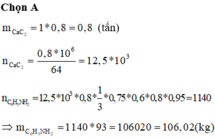


tính theo sơ đồ nhưng không có số % trên sơ đồ không làm được
\(n_{C_2H_2}=\dfrac{2.24\cdot10^3}{22.4}=100\left(mol\right)\)
Dự vào sơ đồ phản ứng :
\(n_{CaCO_3\left(pư\right)}=100\left(mol\right)\)
\(m_{CaCO_3\left(tt\right)}=\dfrac{100\cdot100}{75\%}=13333.33\left(g\right)\)