Điện phân 200ml một dung dịch có chứa hai muối là Cu(NO3)2 và AgNO3 với cường độ dòng điện là 0,804 A, đến khi bọt khí bắt đầu thoát ra ở cực âm thì thời gian điện phàn là 2 giờ, người ta nhận thấy khối lượng cực âm tăng thêm 3,44 g. Hãy xác định nồng độ mol của mỗi muối trong dung dịch ban đầu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
Khi bọt khí bắt đầu thoát ra ở catot là thời điểm Ag+ và Cu2+ đều bị điện phân hết.
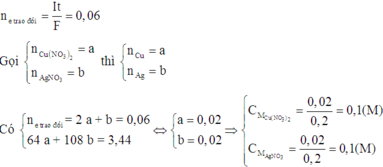

Đáp án C
Catot (−):
C u 2 + + 2 e → C u A g + + 1 e → A g n e = I t n F = 2 n C u + n A g = 0 , 06 m o l m c a t o t t ă n g = m C u + m A g = 4 , 2 g n C u = n C u 2 + = 0 , 015 m o l → C M ( C u 2 + ) = 0 , 075 M

Đáp án : A
Catot(-) :
Cu2+ + 2e -> Cu
Ag+ + 1e -> Ag
ne = It/nF = 2nCu + nAg = 0,06 mol
mcatot tăng = mCu + mAg = 64nCu + 108nAg = 4,2g
=> nCu = n C u 2 + = 0,015 mol
=> C M C u 2 + = 0,075M

Đáp án A.
Theo định luật II của Pha – ra – đây thì khối lượng Cu sinh ra ở catot là:
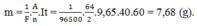
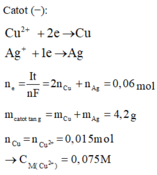




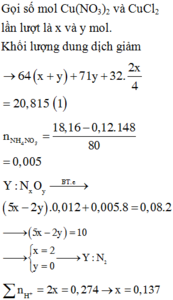
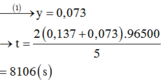
2 giờ = 7200 s
Gọi thời gian điện phân muối bạc là t1
Gọi thời gian điện phân muối đồng là t2
⇒ t1 + t2 = 7200 (1)
Theo định luật Faraday:
mà mAg + mCu = 3,44 (g) ⇒ (9.t1 + 2,666.t2 ). 10-4 = 3,44 (2)
(1),(2) ⇒ t1 = 2400 (s) ⇒ mAg = 2,16 gam ⇒ nAg = 0,02
t2 = 4800 (s) ⇒ mCu = 1,28 gam ⇒ nCu = 0,02
CM Cu(NO3)2 = 0,02/0,2 = 0,1M ; CM AgNO3 = 0,02/0,2 = 0,1 M