hỗn hợp X gồm 0,05 mol O2 và 0,15 mol N2. Tính: -Khối lượng hỗn hợp -Tỉ khối của X với H2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(a.\)
\(n_{hh}=0.2+0.15+0.1=0.45\left(mol\right)\)
\(V_X=0.45\cdot22.4=10.08\left(l\right)\)
\(b.\)
\(m_X=0.2\cdot28+0.15\cdot71+0.1\cdot32=19.45\left(g\right)\)
\(c.\)
\(\overline{M}_X=\dfrac{19.45}{0.45}=43.22\left(g\text{/}mol\right)\)
\(d.\)
\(d_{X\text{/}kk}=\dfrac{43.22}{29}=1.4\)
Nặng hơn không khí 1.4 lần

\(a.\)
\(m_{hh}=0.12\cdot90+0.15\cdot58=19.5\left(g\right)\)
\(b.\)
\(V_{hh}=\left(0.25+0.1+0.05\right)\cdot22.4=8.96\left(l\right)\)
\(c.\)
\(n_A=\dfrac{10.08}{22.4}=0.45\left(mol\right)\)
\(M_A=23\cdot2=46\left(\dfrac{g}{mol}\right)\)
\(m_A=0.45\cdot46=20.7\left(g\right)\)
\(d.\)
\(n_{hh}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
Vì CO2 : O2 = 2 : 1
\(\Rightarrow n_{CO_2}=0.2\left(mol\right),n_{O_2}=0.1\left(mol\right)\)
\(m_{hh}=0.2\cdot44+0.1\cdot32=12\left(g\right)\)
\(\overline{M}=\dfrac{12}{0.3}=40\left(\dfrac{g}{mol}\right)\)

Đáp án C
Đặt ![]()
![]()
![]()
Bảo toàn nguyên tố Oxi:
![]()
Bảo toàn nguyên tố Hidro:
![]()
Bảo toàn điện tích:
![]()
![]()

a) Theo đề ra: \(\left\{{}\begin{matrix}m_{O2}=0,1\cdot32=3,2\left(gam\right)\\m_{N2}=28\cdot0,25=7\left(gam\right)\\m_{CO}=0,15\cdot28=4,2\left(gam\right)\end{matrix}\right.\)
=> \(\overline{M_{tb}}=\dfrac{m_{O2}+m_{N2}+m_{CO}}{n_{O2}+n_{N2}+n_{CO}}=\dfrac{3,2+7+4,2}{0,1+0,25+0,15}=28,8\left(\dfrac{g}{mol}\right)\) b) dhỗn hợp / H2 = \(\dfrac{28,8}{2}=14,4\)
Vậy ....
a) \(\overline{M_{tb}}=\frac{m_{O_2}+m_{N_2}+m_{CO}}{n_{O_2}+n_{N_2}+n_{CO}}\\ =\frac{0,1.32+0,25.28+0,15.28}{0,1+0,25+0,15}\\ =\frac{14,4}{0,5}=28,8\left(\frac{g}{mol}\right)\)
b) \(d_{\frac{hỗnhợp}{KK}}=\frac{28,8}{29}\approx0,993\\ d_{\frac{hỗnhợp}{H_2}}=\frac{28,8}{2}=14,4\)

a, mX = 0,2.32 + 0,15.28 = 10,6 (g)
nX = 0,2 + 0,15 = 0,35 (mol)
=> MX = \(\dfrac{10,6}{0,35}=30,3\left(\dfrac{g}{mol}\right)\)
=> dX/kk = \(\dfrac{30,3}{29}=1,05\)
b, mY = 0,5.44 + 2.2 = 26 (g)
nY = 0,5 + 2 = 2,5 (mol)
=> MY = \(\dfrac{26}{2,5}=10,4\left(\dfrac{g}{mol}\right)\)
=> dY/O2 = \(\dfrac{10,4}{32}=0,325\)
c, mA = 17,75 + 8,4 = 26,15 (g)
nA = \(\dfrac{17,75}{71}+\dfrac{8,4}{28}=0,55\left(mol\right)\)
=> MA = \(\dfrac{26,15}{0,55}=47,6\left(\dfrac{g}{mol}\right)\)
=> dA/CO2 = \(\dfrac{47,6}{44}=1,1\)
Mình làm mẫu 3 ý đầu rồi mấy ý sau bạn tự làm nhé

a) \(\overline{M}_A=5,875.2=11,75\left(g/mol\right)\)
b) Gọi số mol N2, H2 là a, b (mol)
\(\overline{M}_A=\dfrac{28a+2b}{a+b}=11,75\left(g/mol\right)\)
=> 16,25a = 9,75b
=> a = 0,6b
\(\left\{{}\begin{matrix}\%n_{N_2}=\dfrac{a}{a+b}.100\%=\dfrac{0,6b}{0,6b+b}.100\%=37,5\%\\\%n_{H_2}=\dfrac{b}{a+b}.100\%=\dfrac{b}{0,6b+b}.100\%=62,5\%\end{matrix}\right.\)
c)
1 mol hỗn hợp A chứa \(\left\{{}\begin{matrix}n_{N_2}=\dfrac{1.37,5}{100}=0,375\left(mol\right)\\n_{H_2}=\dfrac{1.62,5}{100}=0,625\left(mol\right)\end{matrix}\right.\)
\(\overline{M}_B=\dfrac{0,375.28+0,625.2+17x}{1+x}=6,4.2=12,8\left(g/mol\right)\)
=> x = 0,25 (mol)
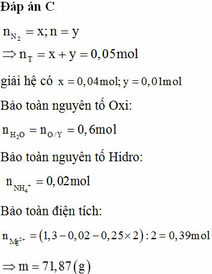
\(m_{hh}=m_{O_2}+m_{N_2}=0.05\cdot32+0.15\cdot28=5.8\left(g\right)\)
\(\overline{M}_X=\dfrac{5.8}{0.05+0.15}=29\left(\dfrac{g}{mol}\right)\)
\(d_{X\text{/}H_2}=\dfrac{29}{2}=14.5\)