Đốt cháy hết (x)g khí C2H4 trong khí Oxi thu đc 11,2 (l) khí CO2 (đktc) và nước. Tính x và thể tích khí Oxi cần dùng (đktc)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a.\(n_{CH_4}=\dfrac{V_{CH_4}}{22,4}=\dfrac{6,72}{22,4}=0,3mol\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
0,3 0,6 ( mol )
\(V_{O_2}=n_{O_2}.22,4=0,6.22,4=13,44l\)
b.
\(n_P=\dfrac{m_P}{M_P}=\dfrac{3,1}{31}=0,1mol\)
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
0,1 0,05 ( mol )
\(m_{P_2O_5}=n_{P_2O_5}.M_{P_2O_5}=0,05.142=7,1g\)

a, Theo giả thiết ta có: \(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\)
\(4P+5O_2--t^o->2P_2O_5\)
Ta có: \(n_{O_2}=\dfrac{5}{4}.n_P=0,125\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=0,125.22,4=2,8\left(l\right)\)
b, Theo giả thiết ta có: \(n_{CH_4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(CH_4+2O_2--t^o->CO_2+2H_2O\)
Ta có: \(n_{O_2}=2.n_{CH_4}=0,1\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=2,24\left(l\right)\)

\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\Rightarrow n_C=0,2mol\Rightarrow m_C=2,4g\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3mol\Rightarrow m_H=0,6g\)
\(\Rightarrow\Sigma m_{CO_2+H_2O}=2,4+0,6=3< m_X\)
Vậy X chứa C,H,O.
\(\Rightarrow m_O=4,6-3=1,6g\Rightarrow n_O=0,1mol\)
Gọi CTHH là \(C_xH_yO_z\)
\(\Rightarrow x:y:z=0,2:0,6:0,1=2:6:1\)
\(\Rightarrow C_2H_6O\)
pthh: \(C_2H_6O+3O_2\underrightarrow{t^o}2CO_2+3H_2O\)
0,3 0,2 0,3
\(V_{O_2}=0,3\cdot22,4=6,72l\)

Đáp án A
Hỗn hợp khí gồm CH4, C2H6 và C3H8 là các hidrocacbon.
Mà khi đốt cháy 1 hidrocacbon bất kì ta luôn có:
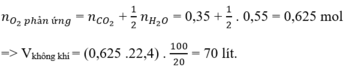


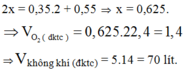
\(n_{CO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: C2H4 + 3O2 --to--> 2CO2 + 2H2O
0,25<--0,75<------0,5
=> \(\left\{{}\begin{matrix}m_{C_2H_4}=0,25.28=7\left(g\right)\\V_{O_2}=0,75.22,4=16,8\left(l\right)\end{matrix}\right.\)