Một oxit kim loại chứa 52,94% kim loại (về khối lượng). Hãy XĐ công thức phân tử của oxit đó
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi công thức oxit là \(R_xO_y\)
\(M_{R_xO_y}=Rx+16y=102\)
\(\%R=\frac{Rx.100}{Rx+16y}\)
\(\Leftrightarrow52,94=\frac{Rx.100}{102}\)
\(\Leftrightarrow Rx=\frac{52,94.102}{100}\approx54\)
\(\Leftrightarrow R=\frac{54}{x}\)
Với \(x=1\Rightarrow R=54\left(l\right)\)
Với \(x=2\Rightarrow R=27\left(Al\right)\)
Với \(x=3\Rightarrow R=18\left(l\right)\)
Vậy công thức oxit cần tìm là \(Al_2O_3\)
(Không chắc)

Đặt công thức của oxit kim loại là MxOy
%mO = 100% - 70% = 30%
⇒ mO = 12y = 160.30% = 48
⇒ y = 3
mM = 160.70% = 112g = M.x (với M là phân tử khối của kim loại M)
Áp dụng quy tắc hóa trị ta có:
a.x = 2.3 = 6 (với a là hóa trị của M; a = 1; 2; 3)
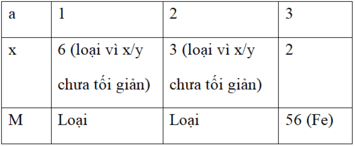
⇒ M là kim loại Sắt.
Vậy công thức hóa học của oxit kim loại là Fe2O3 (Sắt (III) oxit).

1)
PTKR2Ox = 2.NTKR + 16x = 102 (đvC)
| x | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| NTKR | 43(Loại) | 35(Loại) | 27(Al) | 19(Loại) | 11(Loại) | 3(Loại) | Loại | Loại |
=> R là Al
2)
CTHH: RxOy
\(\%R=\dfrac{x.NTK_R}{160}.100\%=70\%\)
=> \(NTK_R=\dfrac{112}{x}\left(đvC\right)\)
Chỉ có x = 2 thỏa mãn \(NTK_R=\dfrac{112}{2}=56\left(đvC\right)\)
=> R là Fe
PTKFe2Oy = 160 (đvC)
=> y = 3
CTHH: Fe2O3

Khối lượng của kim loại có trong oxit kim loại:
MKL = 112 g
Khối lượng nguyên tố oxi: mO = 160 – 112 = 48g
Đặt công thức hóa học của oxit kim loại là MxOy, ta có:
MKL. x = 112 => nếu x = 2 thì M = 56. Vậy M là Fe
16y = 48 => y = 3
Vậy CTHH: Fe2O3, đó là sắt (III) oxit
Hoan hô , Học sinh tự hỏi tự trả lời
Hoan hô oooooooooooooooooooooooooooo
CTHH: RxOy
Có \(\%R=\dfrac{x.M_R}{x.M_R+16y}.100\%=52,94\%=>M_R=9.\dfrac{2y}{x}\)(g/mol)
Xét \(\dfrac{2y}{x}=1=>L\)
Xét \(\dfrac{2y}{x}=2=>L\)
Xét \(\dfrac{2y}{x}=3=>M_R=27\left(Al\right)=>\dfrac{x}{y}=\dfrac{2}{3}=>Al_2O_3\)