Cho 10,5 gam hỗn hợp Mg, Al (tie lệ mol là 1:3) vào 250ml dung dịch CuCl2 1M. Khuấy kĩ cho phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Tính giá trị m?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án : D
mAl + mFe = 5,5 và nAl =2nFe
=>nAl = 0,1 ; nFe = 0,05 mol
,nAgNO3 = 0,3 mol
Al + 3AgNO3 -> Al(NO3)3 + 3Ag
=> chất rắn gồm 0,3 molAg và 0,05 mol Fe
=> m = 35,2g

Gọi nFe = x (mol) ⇒ nAl = 2nFe = 2x (mol)
mhỗn hợp= 56x + 2x. 27 = 5,5⇒ x = 0,05 (mol)⇒ nFe = 0,05 (mol), nAl = 0,1 (mol)
nAgNO3 = 0,3.1 = 0,3 (mol)
Viết PTHH có xảy ra theo thứ tự:
Al + 3AgNO3 → Al(NO3)3 + 3Ag↓ (1)
Fe + 3AgNO3 → Fe(NO3)2+ 3Ag↓ (2)
Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag↓ (3)
nAl = 0,1 (mol); nAgNO3 = 0,3 (mol) ⇒ chỉ xảy ra phản ứng (1). Không xảy ra phản ứng (2) và (3)
⇒m rắn = mAg↓ + mFe dư = 3*0,1*108 + 0,05*56 = 35,2 (g)

Do nAl : nFe = 2 : 1 và 27nAl + 56nFe = 7,15g
=> nAl = 0,13 mol ; nFe = 0,065 mol
nAgNO3 = 0,39 mol. Phản ứng xảy ra :
+/ Al + 3Ag+ → Al3+ + 3Ag
=>sau phản ứng có 0,39 mol Ag và 0,065 mol Fe
=> m = 45,76g
=>C

Chọn B
Gọi số mol Fe là x => số mol Al là 2x
Ta có: 56x + 27.2x = 5,5 => x = 0,05; = 0,3.1 = 0,3 (mol)
Al + 3Ag+ → Al3+ + 3Ag
0,1 0,3 0,3 (mol)
Vậy chất rắn thu được gồm Fe và Ag; m = 0,05.56 + 108.0,3 = 35,2 (gam).
Cho 5,5 gam hỗn hợp bột Al và Fe ( tỉ lệ mol 2:1) vào 330 ml dung dịch AgNO31M. Khuấy kĩ cho oharn ứng xẩy ra hoàn toàn thu được m gam chất rắn. Giá trị của m là
A. 33,95 gam
B. 35,20 gam
C. 39,35 gam
D. 35,39 gam

a) Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Al}=2a\left(mol\right)\end{matrix}\right.\left(a>0\right)\Rightarrow56a+27.2a=11\Leftrightarrow a=0,1\left(mol\right)\left(TM\right)\)
PTHH:
Al + 3AgNO3 ---> Al(NO3)3 + 3Ag
0,2->0,6--------->0,2---------->0,6
Fe + 2AgNO3 ---> Fe(NO3)2 + 2Ag
0,05<-0,1--------->0,05-------->0,1
=> \(m_{c.r\text{ắn}}=m_{Ag}+m_{Fe\left(d\text{ư}\right)}=0,7.108+0,05.56=78,4\left(g\right)\)
b) \(\left\{{}\begin{matrix}C_{M\left(Al\left(NO_3\right)_3\right)}=\dfrac{0,2}{0,7}=\dfrac{2}{7}M\\C_{M\left(Fe\left(NO_3\right)_2\right)}=\dfrac{0,05}{0,7}=\dfrac{1}{14}M\end{matrix}\right.\)

Để xử lý bài toán này ta có thể hiểu theo kiểu nông dân. Số mol anion sẽ được phân bổ cho các kim loại từ mạnh nhất tới yếu hơn. Hết anion thì bọn kim loại yếu sẽ bị đẩy ra ngoài.
Ta có
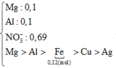
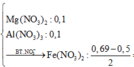
=0,095
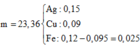

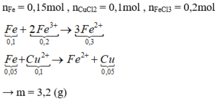
\(\left\{{}\begin{matrix}24n_{Mg}+27n_{Al}=10,5\\\dfrac{n_{Mg}}{n_{Al}}=\dfrac{1}{3}\end{matrix}\right.=>\left\{{}\begin{matrix}n_{Mg}=0,1\\n_{Al}=0,3\end{matrix}\right.\)
\(n_{CuCl_2}=0,25.1=0,25\left(mol\right)\)
PTHH: Mg + CuCl2 --> MgCl2 + Cu
0,1--->0,1----------------->0,1
2Al + 3CuCl2 --> 2AlCl3 + 3Cu
0,1<---0,15----------------->0,15
=> \(\left\{{}\begin{matrix}n_{Al}=0,2\left(mol\right)\\n_{Cu}=0,25\left(mol\right)\end{matrix}\right.\)
=> m = 0,2.27 + 0,25.64 = 21,4 (g)
\(\left\{{}\begin{matrix}24.n_{Mg}+27.n_{Al}=10,5\\\dfrac{n_{Mg}}{n_{Al}}=\dfrac{1}{3}\end{matrix}\right.=>\left\{{}\begin{matrix}n_{Mg}=0,1\\n_{Al}=0,3\end{matrix}\right.\)
\(n_{CuCl_2}=0,25.1=0,25\left(mol\right)\)
PTHH: Mg + CuSO4 --> MgSO4 + Cu
0,1--->0,1-------->0,1------>0,1
2Al + 3CuSO4 --> Al2(SO4)3 + 3Cu
0,1<-0,15--------------------->0,15
=> \(\left\{{}\begin{matrix}n_{Al}=0,3-0,1=0,2\left(mol\right)\\n_{Cu}=0,25\left(mol\right)\end{matrix}\right.=>m=0,2.27+0,25.64=21,4\left(g\right)\)