Đốt cháy hoàn toàn 4,44g hỗn hợp Al và Fe trong khí oxi. Sau phản ứng kết thúc thu được chất rắn A. Cho dòng khí H2 dư đi qua A nung nóng cho tới khi các phản ứng xảy ra hoàn toàn thu được 5,4g chất rắn B. Tính khối lượng mỗi kim loại có trong hỗn hợp ban đầu.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3\\ 3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4\\ Fe_3O_4 + 4H_2 \xrightarrow{t^o} 3Fe + 4H_2O\\ Ta\ có :\\ m_O = m_B - m_{hh} = 5,4 - 4,44 = 0,96(mol)\\ n_O = \dfrac{0,96}{32} = 0,03(mol)\\ \Rightarrow n_{Al_2O_3}= \dfrac{1}{3}n_O = 0,01(mol)\\ \Rightarrow n_{Al} = 2n_{Al_2O_3} = 0,02(mol)\\ m_{Al} = 0,02.54 = 1,08(gam)\\ m_{Fe} = 4,44 - 1,08 = 3,36(gam)\)

Đáp án C
Ta có nO bị lấy đi bởi CO = 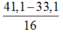 = 0,5 mol
= 0,5 mol
⇒ nCO pứ = nO = 0,5 mol
Bảo toàn e cả quá trình ta có: 2nCO = 2nH2 Û nH2 = nCO = 0,5 mol
⇒ VH2 = 0,5 × 22,4 = 11,2 lít

Gọi \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\left(đk:a,b>0\right)\)
PTHH:
\(4Al+3O_2\xrightarrow[]{t^o}2Al_2O_3\)
b--------------->0,5b
\(2Mg+O_2\xrightarrow[]{t^o}2MgO\)
a---------------->a
\(\rightarrow\left\{{}\begin{matrix}24a+27b=5,1\\40a+102b=9,1\end{matrix}\right.\Leftrightarrow a=b=0,1\left(mol\right)\left(TM\right)\)\
PTHH:
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
0,1----------------------------->0,1
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)+3H_2\uparrow\)
0,1----------------------------------->0,15
=> V = (0,1 + 0,15).22,4 = 5,6 (l)
Ở trên Al2O3 là 0,5b (mol) mà sao xuống dưới Al2O3 b(mol) em?

Đáp án D.
CO khử được các oxit kim loại của kim loại đứng sau Al trong dãy điện hóa thành kim loại và khí CO2.
=> CO chỉ khử được CuO thành Cu; Al2O3 và MgO không bị khử.

a) PTHH : \(2Al+6HCl-->2AlCl_3+3H_2\) (1)
\(Fe+2HCl-->FeCl_2+H_2\) (2)
\(H_2+CuO-t^o->Cu+H_2O\) (3)
b) Ta có : \(m_{CR\left(giảm\right)}=m_{O\left(lay.di\right)}\)
=> \(m_{O\left(lay.di\right)}=32-26,88=5,12\left(g\right)\)
=> \(n_{O\left(lay.di\right)}=\frac{5,12}{16}=0,32\left(mol\right)\)
Theo pthh (3) : \(n_{H_2\left(pứ\right)}=n_{O\left(lay.di\right)}=0,32\left(mol\right)\)
=> \(tổng.n_{H_2}=\frac{0,32}{80}\cdot100=0,4\left(mol\right)\)
Đặt \(\hept{\begin{cases}n_{Al}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{cases}}\) => \(27a+56b=11\left(I\right)\)
Theo pthh (1) và (2) : \(n_{H_2\left(1\right)}=\frac{3}{2}n_{Al}=\frac{3}{2}a\left(mol\right)\)
\(n_{H_2\left(2\right)}=n_{Fe}=b\left(mol\right)\)
=> \(\frac{3}{2}a+b=0,4\left(II\right)\)
Từ (I) và (II) => \(\hept{\begin{cases}a=0,2\\b=0,1\end{cases}}\)
=> \(\hept{\begin{cases}m_{Al}=27\cdot0,2=5,4\left(g\right)\\m_{Fe}=56\cdot0,1=5,6\left(g\right)\end{cases}}\)
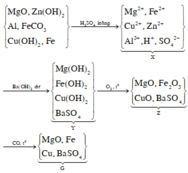
Gọi $n_{Al}= a(mol) ; n_{Fe} = b(mol) \Rightarrow 27a + 56b = 4,44(1)$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
$3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4$
$Fe_3O_4 + 4H_2 \xrightarrow{t^o} 3Fe + 4H_2O$
B gồm : $Al_2O_3, Fe$
$n_{Al_2O_3} = \dfrac{1}{2}n_{Al} = 0,5a(mol)$
Suy ra: $0,5a.102 + 56b = 5,4(2)$
Từ (1)(2) suy ra a = 0,04 ; b = 0,06
$m_{Al} = 0,04.27 =1,08\ gam$
$m_{Fe} = 0,06.56 = 3,36\ gam$