Đá vôi là nguyên liệu để sản xuất vôi sống có thành phần chính là Canxi cacbonat.
b) Tính số nguyên tử Oxi có trong 50g hợp chất
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: MCaCO3 = 40 + 12 + (16 × 3) = 100g
Trong 1mol CaCO3 có 1mol Ca, 1 mol C và 3 mol O
Do đó: MCa = 1 × 40 = 40g
MC = 1 × 12 = 12g
MO = 3 × 16 = 48g
Thành phần % các nguyên tố có trong hợp chất CaCO3 là:
%Ca = (40/100) × 100% = 40%
%C = (12/100) × 100% = 12%
%O = (16 × 3/100) × 100% = 48%
Vậy ....

`- CaSO_4`
`K.L.P.T = 40 + 32 + 16.4 = 136 <am``u>`
\(\%Ca=\dfrac{40.100}{136}\approx29,41\%\)
`- CaCO_3`
`K.L.P.T = 40 + 12 + 16.3 = 100 <am``u>`
\(\%Ca=\dfrac{40.100}{100}=40\%\)
`- CaCl_2`
`K.L.P.T = 40 + 35,5.2=75,5 <am``u>`
\(\%Ca=\dfrac{40.100}{75,5}\approx52,98\%\)

a) Đá vôi (thành phần chính là chất canxi cacbonat) được đập thành cục nhỏ tương đối đều nhau.
=> Hiện tượng vật lý
Sau đó đá vôi được xếp vào lò nung nóng thì thu được vôi sống (chất canxi oxit), và khí cacbon đioxit thoát ra.
=> Hiện tượng hóa học
b) Canxi cacbonat ---to→ Canxi oxit + Cacbon đioxit
c) \(Tacó:M_{Ca\left(HXO_3\right)_2}=162\\ \Rightarrow40+\left(1+M_X+16.3\right).2=162\\ \Rightarrow M_X=12\)
=> X là Cacbon (C)
a, HT vật lí: Đập thành cục nhỏ
HT hoá học: Nung nóng đá vôi
b) Canxi cacbonat ----to---> Vôi sống + Khí cacbonic
c)
\(PTK_{Ca\left(HXO_3\right)_2}=162\left(\text{đ}.v.C\right)\\ \Leftrightarrow40+49.2+2.NTK_X=162\\ \Leftrightarrow NTK_X=12\left(\text{đ}.v.C\right)\\ \Rightarrow X:Cacbon\left(C=12\right)\\ \Rightarrow CTHH:Ca\left(HCO_3\right)_2\)
Tên: Canxi bicacbonat/ Canxi hidrocacbonat

Giai đoạn: Đá vôi đập thành cục nhỏ. Hiện tượng vật lí vì đá vôi biến đổi hình dạng.
Giai đoạn 2: Đá vôi nung nóng thu được vôi sống và khí cacbon đioxit là hiện tượng hóa học vì đá vôi đã biến đổi thành chất khác.

a) mCaCO3 = mCaO + mCO2
b) Khối lượng của CaCO3 đã phản ứng:
140 + 110 = 250 kg
Tỉ lệ phần trăm khối lượng CaCO3 chứa trong đá vôi:
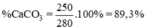

\(CaCO_3\underrightarrow{t^o}CaO+CO_2\uparrow\)
nCaO = 33,6/56 = 0,6 (mol)
nCO2 = 26,4/44 = 0,6 (mol)
=> nCaCO3 = 0,6 mol <=> mCaCO3 = 0,6.100 = 60 (g)

- Phân tử calcium carbonate = 1 nguyên tử calcium + 1 nguyên tử carbon + 3 nguyên tử oxygen
=> Khối lượng phân tử calcium carbonate = 40 amu x 1 + 12 amu x 1 + 16 amu x 3 = 100 amu
- Ứng dụng của đá vôi là:
+ Sản xuất vôi sống
+ Chế biến thành chất độn dùng trong sản xuất xà phòng
+ Sản xuất xi măng
+ Dùng làm chất bó bột trong y học
+ Là chất làm nền cho các loại thuốc viên

\(PTK_{CaCO_3}=NTK_{Ca}+NTK_C+3.NTK_O=40+12+3.16=100\left(đ.v.C\right)\\ \%m_{Ca}=\dfrac{NTK_{Ca}}{PTK_{CaCO_3}}.100\%=\dfrac{40}{100}.100=40\%\\ \%m_C=\dfrac{NTK_C}{PTK_{CaCO_3}}.100\%=\dfrac{12}{100}.100=12\%\\ \%m_O=100\%-\left(\%m_{Ca}+\%m_C\right)=100\%-\left(40\%+12\%\right)=48\%\)

PTHH: CaCO3 ---to→ CaO + CO2
Theo ĐLBTKL ta có: \(m_{CaCO_3}=m_{CaO}+m_{CO_2}=140+110=250\left(kg\right)\)
\(\%m_{CaCO_3}=\dfrac{250.100\%}{300}=83,33\%\)
\(b,n_{CaCO_3}=\dfrac{m}{M}=\dfrac{50}{100}=0,5(mol)\\ \Rightarrow n_O=3n_{CaCO_3}=1,5(mol)\\ \Rightarrow \text{Số nguyên tử oxi là: }A_O=1,5.6.10^{23}=9.10^{23}\)
Ta có: \(n_{CaCO_3}=\dfrac{50}{100}=0,5\left(mol\right)\)
\(\Rightarrow n_O=0,5.3=1,5\left(mol\right)\)
Vậy số nguyên tử oxi là: \(SNT_O=1,5.6.10^{23}=9,10^{23}\left(phân.tử\right)\)