Giúp em với. Em cần lời giải chi tiết
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



3:
a: x+4/7=19/14
=>x=19/14-4/7=19/14-8/14=11/14
b: x*4/15=-3/10
=>x=-3/10:4/15=-3/10*15/4=-45/40=-9/8
c: 23,4-x=1,3
=>x=23,4-1,3=22,1
4:
a: B nằm giữa A và C
b: MA,MB,MC,AC

Câu 40. \(n_{NaOH}=\dfrac{20}{40}=0,5\left(mol\right);n_{HCl}=\dfrac{36,5}{36,5}=1\left(mol\right)\)
PTHH: \(NaOH+HCl\rightarrow NaCl+H_2O\)
Theo đề: 0,5mol .....1mol
Lập tỉ lệ : \(\dfrac{0,5}{1}< \dfrac{1}{1}\)=> Sau phản ứng NaOH hết, HCl dư
=> Thử môi trường sau phản ứng bằng quỳ sẽ có màu đỏ
Câu 41.
nNaOH=0,3.0,5=0,15(mol);nHCl=0,3.1=0,3(mol)
PTHH: NaOH + HCl → NaCl + H2O
Theo đề:0,15mol ....0,3mol
Lập tỉ lệ :\(\dfrac{0,15}{1}< \dfrac{0,3}{1}\)=> Sau phản ứng NaOH hết, HCl dư
=> Dung dịch sau phản ứng làm quỳ tím hóa màu đỏ

Khối lượng của hợp kim đó :
\(8,5:\dfrac{5}{8}=13,6\left(kg\right)\)





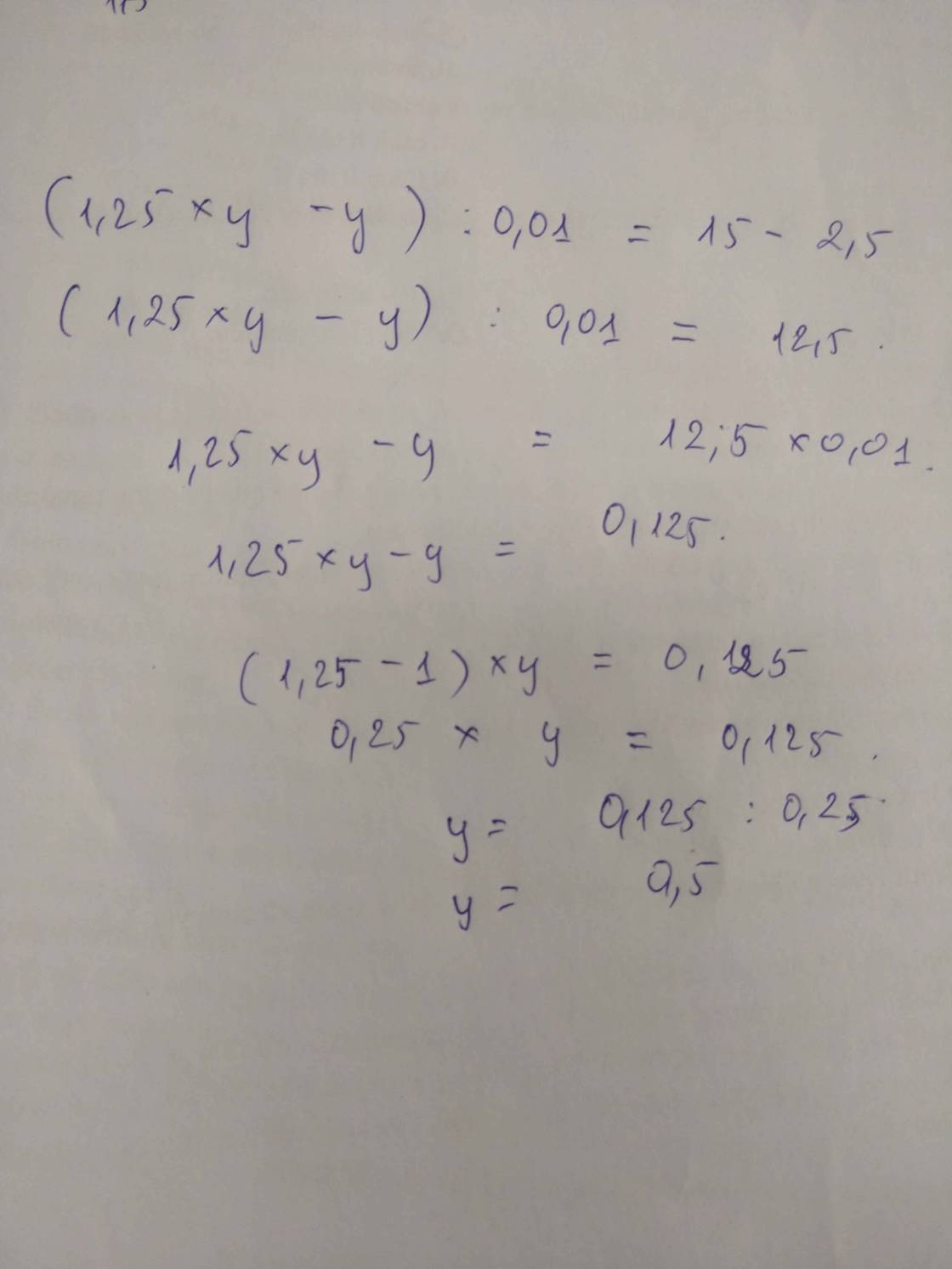

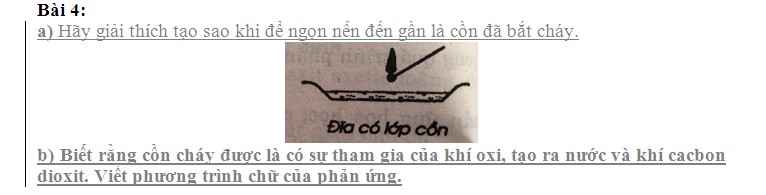 mấy anh chị giải chi tiết giùm em,em cần lời giải chi tiết ạ em xin cảm ơn
mấy anh chị giải chi tiết giùm em,em cần lời giải chi tiết ạ em xin cảm ơn

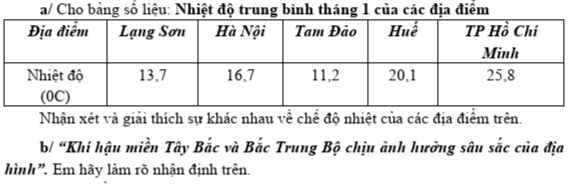

a.2Al + 6HCl -> 2AlCl3 + 3H2
2a 6a 3a
Fe + 2HCl -> FeCl2 + H2
b 2b b
b.\(nH2=\dfrac{1.344}{22.4}=0.06mol\)
Ta có hệ phương trình: \(\left\{{}\begin{matrix}54a+56b=2.22\\3a+b=0.06\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0.01mol\\b=0.03mol\end{matrix}\right.\)
\(\%mAl=\dfrac{0.01\times2\times27\times100}{2.22}=24.3\%\)
%mFe = 100 - 24.3 =75.7%
c.nHCl = 6a + 2b = 0.12 mol
\(CM_{HCl}=\dfrac{0.12}{0.2}=0.6M\)